Pirtobrutinib
ピルトブルチニブ (ジャイパーカ®)
ジャイパーカ®は従来、 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫に適応を有していたが、 2025年9月19日に 「他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性の慢性リンパ性白血病 (小リンパ球性リンパ腫を含む) 」 が追加承認された。
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ジャイパーカ® (ピルトブルチニブ)
*日本新薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】最小~軽度*
【FN発症】低リスク**
*嘔吐頻度<30% (NCCN Guidelines Version 2.2025 Antiemesis)
**BRUIN CLL-321のFN発現率0.9%²⁾を基に編集部が分類
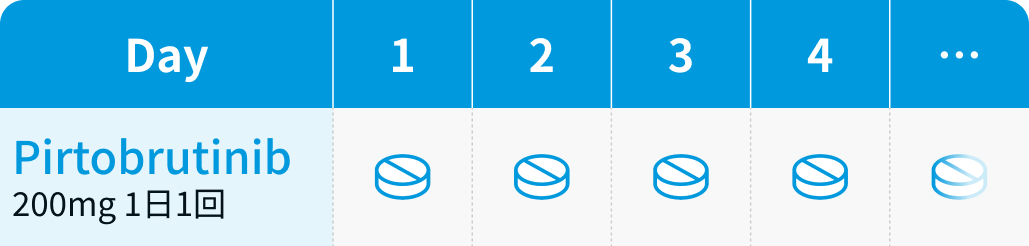
成人にはピルトブルチニブとして200mgを1日1回経口投与
Key Data|臨床試験結果
📊 BRUIN CLL-321試験
J Clin Oncol. 2025;43(22):2538-2549.
過去に共有結合型ブルトン型チロシンキナーゼ (BTK) 阻害薬治療歴のある再発・難治性慢性リンパ性白血病 (CLL) /小リンパ球性リンパ腫 (SLL) 患者238例を対象とした第III相無作為化比較試験。 患者はピルトブルチニブ群または医師選択治療群*に1:1で割り付けられ、 主要評価項目はPFSとされた。
*Idelalisib+RituximabまたはBendamustine+Rituximab
【有効性】ピルトブルチニブ (vs 医師選択治療)
EFS : event-free survival、 TTNT : time to next treatment or death、 VEN : ベネトクラクス
- PFS中央値 14.0ヵ月 (vs 8.7ヵ月)
- HR 0.54 (95%CI 0.39–0.75)
- OS中央値 29.7ヵ月 (vs 未到達)
- HR 1.09 (95%CI 0.68–1.75)
- EFS中央値 14.1ヵ月 (vs 7.6ヵ月)
- HR 0.39 (95%CI 0.28–0.53)
- TTNT中央値 24.0ヵ月 (vs 10.9ヵ月)
- HR 0.37 (95%CI 0.25–0.52)
VEN未治療 : HR 0.36 (95%CI 0.21–0.61)
VEN既治療 : HR 0.37 (95%CI 0.23–0.60)
- 全奏効率 69% (vs 50%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 貧血 19.8% (11.2%)
- 肺炎 22.4% (15.5%)
- 好中球減少 18.1% (14.7%)
- 下痢 16.4% (0%)
- 咳嗽 16.4% (0%)
- COVID-19 12.9% (0%)
- 発熱 12.9% (0.9%)
- 倦怠感 11.2% (1.7%)
- 悪心 11.2% (0.9%)
- 嘔吐 6.9% (0.9%)
- ALT上昇 3.4% (0.9%)
- 体重減少 3.4% (0%)
- 貧血/鉄欠乏性貧血 20.7% (11.2%)
- 心房細動/粗動 2.6% (1.7%)
- 出血 21.6% (3.4%)
- 皮下出血 7.8% (0.9%)
- 点状出血/紫斑 5.2% (0.9%)
- 出血性事象 15.5% (2.6%)
- 高血圧 6.9% (2.6%)
- 感染症 (COVID-19除く) 57.8% (22.4%)
- 血小板減少 9.5% (7.8%)
各プロトコル
適格基準
BRUIN CLL-321試験³⁾の主な適格基準:
- 18歳以上 (日本人は20歳以上)
- ECOG PS 0–2
- 好中球≧750/μL
- 血小板≧5万/μL
- ヘモグロビン≧8g/dL
- 腎機能 : CrCl≧30mL/min
- 肝機能 : AST/ALT≦3×ULN、 T-Bil≦1.5×ULN
直近6ヵ月以内のリヒター転換やCNS浸潤歴、 BTK阻害薬による重度出血歴、 心筋梗塞3ヵ月以内、 LVEF≦40%、 NYHA III/IV心不全、 重度不整脈、 持続QTcF延長 (470ms超)、 ワルファリン内服中、 強力なCYP3A4阻害薬/誘導薬使用例等は除外された。
用量レベル
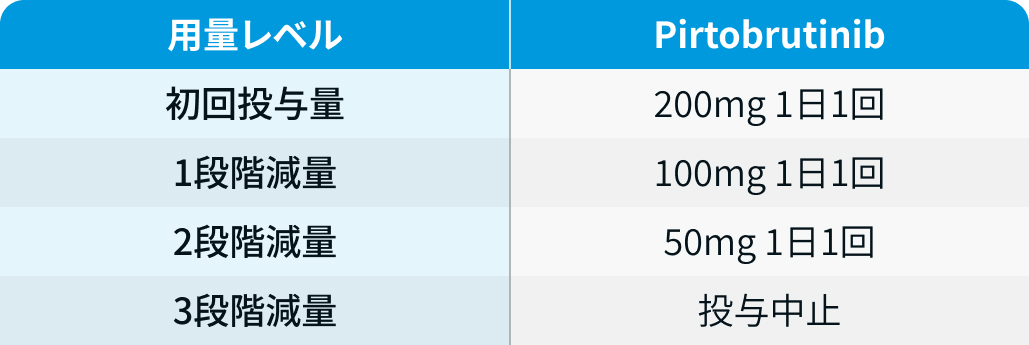
ジャイパーカ®電子添文¹⁾を基に編集部作成
腎障害患者に対する用量調整
尿中未変化体の排泄率は10%であり、 腎障害患者における用量調整は不要と考えられる。
ジャイパーカ®インタビューフォームを基に編集部が評価
有害事象発現時の減量・休薬・中止基準
BRUIN CLL-321試験³⁾では、 有害事象発現時の対応は以下のように規定されていた。
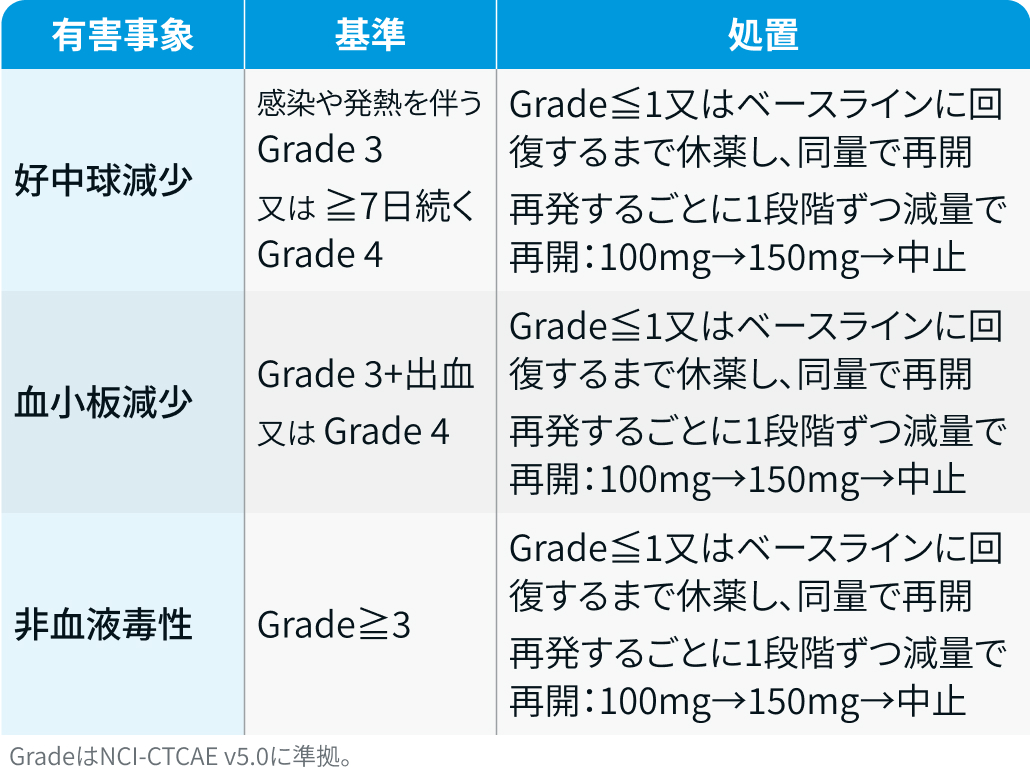
BRUIN CLL-321試験³⁾のプロトコルを基に編集部作成
なお、 ジャイパーカ®電子添文¹⁾では、 Grade≧3の副作用発現時はGrade≦1またはベースラインに回復するまで休薬し、 同量で再開、 再発時は1段階減量することが規定されている。
レジメンの特徴と注意点
🧑⚕️ジャイパーカ®は、 共有結合型BTK阻害剤使用後にC481S変異が生じた場合でもBTK経路を阻害可能な非共有結合型BTK阻害剤であり、 マントル細胞リンパ腫に続いて承認されました。
東海大学医学部 血液腫瘍内科 扇屋大輔先生
作用機序の特徴
ピルトブルチニブは、 B細胞受容体シグナルの下流分子であるBTKを阻害する低分子薬である。 共有結合型BTK阻害薬に対する耐性の原因となるC481変異BTKにも非共有結合かつ可逆的に作用し、 その活性を抑制する。 さらに、 高い経口吸収性と約19時間の半減期を有し、 BTKのターンオーバーに依存せず持続的阻害が可能で、 B細胞腫瘍の増殖抑制に寄与すると考えられる⁴⁾。
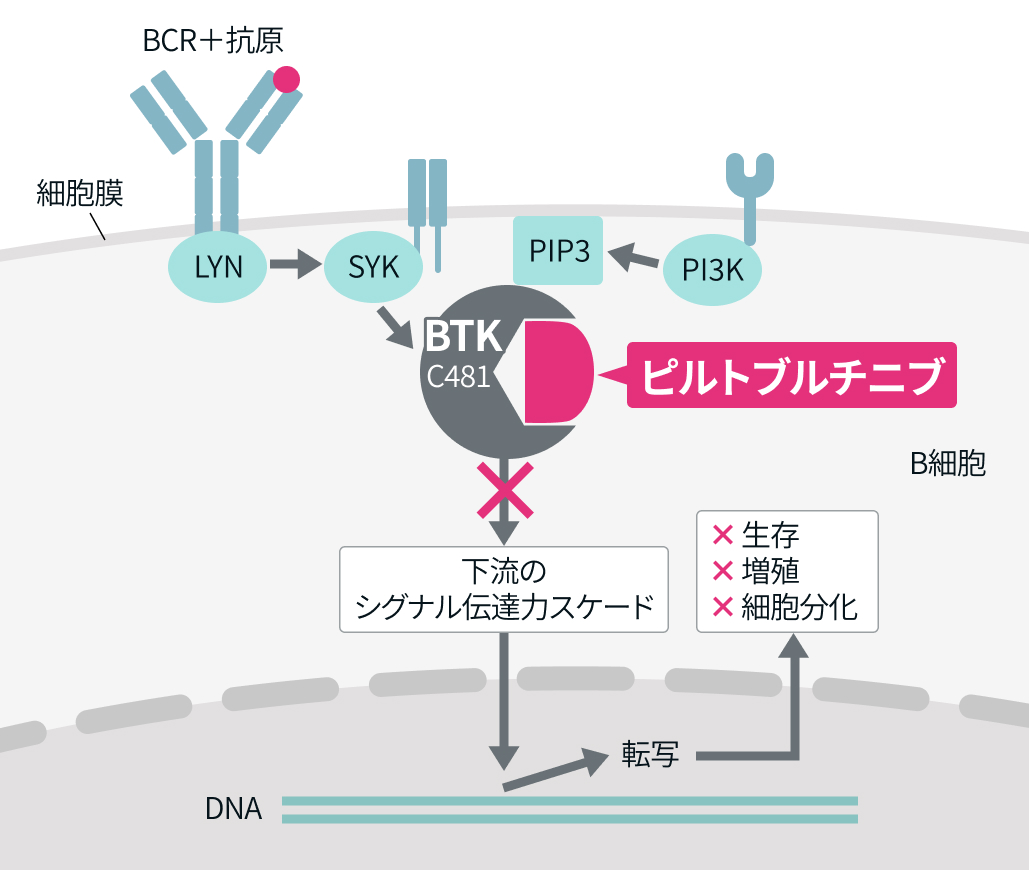
日本新薬株式会社の医療関係者向けサイトの図を基に作図
レジメン適用時の注意事項
出血 : 出血が発現することがあり、 外科的処置では大量出血の可能性があるため、 手術や侵襲的手技を行う際は術前後3–5日程度の休薬を考慮する。
RMP【重要な特定されたリスク】
ジャイパーカ®医薬品リスク管理計画書 (RMP)
- 感染症
- 出血
- 骨髄抑制
出典
- 日本イーライリリー株式会社. ジャイパーカ錠50mg/ジャイパーカ錠100mg 電子添文 2025年9月改訂第3版
- 日本新薬株式会社. ジャイパーカ錠 適正使用ガイド 2025年9月改訂
- J Clin Oncol. 2025;43(22):2538-2549.
- N Engl J Med. 2023:389:33-44.
最終更新 : 2025年9月22日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Pirtobrutinib
ジャイパーカ®は従来、 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫に適応を有していたが、 2025年9月19日に 「他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性の慢性リンパ性白血病 (小リンパ球性リンパ腫を含む) 」 が追加承認された。
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ジャイパーカ® (ピルトブルチニブ)
*日本新薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】最小~軽度*
【FN発症】低リスク**
*嘔吐頻度<30% (NCCN Guidelines Version 2.2025 Antiemesis)
**BRUIN CLL-321のFN発現率0.9%²⁾を基に編集部が分類

成人にはピルトブルチニブとして200mgを1日1回経口投与
Key Data|臨床試験結果
📊 BRUIN CLL-321試験
J Clin Oncol. 2025;43(22):2538-2549.
過去に共有結合型ブルトン型チロシンキナーゼ (BTK) 阻害薬治療歴のある再発・難治性慢性リンパ性白血病 (CLL) /小リンパ球性リンパ腫 (SLL) 患者238例を対象とした第III相無作為化比較試験。 患者はピルトブルチニブ群または医師選択治療群*に1:1で割り付けられ、 主要評価項目はPFSとされた。
*Idelalisib+RituximabまたはBendamustine+Rituximab
【有効性】ピルトブルチニブ (vs 医師選択治療)
EFS : event-free survival、 TTNT : time to next treatment or death、 VEN : ベネトクラクス
- PFS中央値 14.0ヵ月 (vs 8.7ヵ月)
- HR 0.54 (95%CI 0.39–0.75)
- OS中央値 29.7ヵ月 (vs 未到達)
- HR 1.09 (95%CI 0.68–1.75)
- EFS中央値 14.1ヵ月 (vs 7.6ヵ月)
- HR 0.39 (95%CI 0.28–0.53)
- TTNT中央値 24.0ヵ月 (vs 10.9ヵ月)
- HR 0.37 (95%CI 0.25–0.52)
VEN未治療 : HR 0.36 (95%CI 0.21–0.61)
VEN既治療 : HR 0.37 (95%CI 0.23–0.60)
- 全奏効率 69% (vs 50%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 貧血 19.8% (11.2%)
- 肺炎 22.4% (15.5%)
- 好中球減少 18.1% (14.7%)
- 下痢 16.4% (0%)
- 咳嗽 16.4% (0%)
- COVID-19 12.9% (0%)
- 発熱 12.9% (0.9%)
- 倦怠感 11.2% (1.7%)
- 悪心 11.2% (0.9%)
- 嘔吐 6.9% (0.9%)
- ALT上昇 3.4% (0.9%)
- 体重減少 3.4% (0%)
- 貧血/鉄欠乏性貧血 20.7% (11.2%)
- 心房細動/粗動 2.6% (1.7%)
- 出血 21.6% (3.4%)
- 皮下出血 7.8% (0.9%)
- 点状出血/紫斑 5.2% (0.9%)
- 出血性事象 15.5% (2.6%)
- 高血圧 6.9% (2.6%)
- 感染症 (COVID-19除く) 57.8% (22.4%)
- 血小板減少 9.5% (7.8%)
各プロトコル
適格基準
BRUIN CLL-321試験³⁾の主な適格基準:
- 18歳以上 (日本人は20歳以上)
- ECOG PS 0–2
- 好中球≧750/μL
- 血小板≧5万/μL
- ヘモグロビン≧8g/dL
- 腎機能 : CrCl≧30mL/min
- 肝機能 : AST/ALT≦3×ULN、 T-Bil≦1.5×ULN
直近6ヵ月以内のリヒター転換やCNS浸潤歴、 BTK阻害薬による重度出血歴、 心筋梗塞3ヵ月以内、 LVEF≦40%、 NYHA III/IV心不全、 重度不整脈、 持続QTcF延長 (470ms超)、 ワルファリン内服中、 強力なCYP3A4阻害薬/誘導薬使用例等は除外された。
用量レベル

ジャイパーカ®電子添文¹⁾を基に編集部作成
腎障害患者に対する用量調整
尿中未変化体の排泄率は10%であり、 腎障害患者における用量調整は不要と考えられる。
ジャイパーカ®インタビューフォームを基に編集部が評価
有害事象発現時の減量・休薬・中止基準
BRUIN CLL-321試験³⁾では、 有害事象発現時の対応は以下のように規定されていた。

BRUIN CLL-321試験³⁾のプロトコルを基に編集部作成
なお、 ジャイパーカ®電子添文¹⁾では、 Grade≧3の副作用発現時はGrade≦1またはベースラインに回復するまで休薬し、 同量で再開、 再発時は1段階減量することが規定されている。
レジメンの特徴と注意点
🧑⚕️ジャイパーカ®は、 共有結合型BTK阻害剤使用後にC481S変異が生じた場合でもBTK経路を阻害可能な非共有結合型BTK阻害剤であり、 マントル細胞リンパ腫に続いて承認されました。
東海大学医学部 血液腫瘍内科 扇屋大輔先生
作用機序の特徴
ピルトブルチニブは、 B細胞受容体シグナルの下流分子であるBTKを阻害する低分子薬である。 共有結合型BTK阻害薬に対する耐性の原因となるC481変異BTKにも非共有結合かつ可逆的に作用し、 その活性を抑制する。 さらに、 高い経口吸収性と約19時間の半減期を有し、 BTKのターンオーバーに依存せず持続的阻害が可能で、 B細胞腫瘍の増殖抑制に寄与すると考えられる⁴⁾。

日本新薬株式会社の医療関係者向けサイトの図を基に作図
レジメン適用時の注意事項
出血 : 出血が発現することがあり、 外科的処置では大量出血の可能性があるため、 手術や侵襲的手技を行う際は術前後3–5日程度の休薬を考慮する。
RMP【重要な特定されたリスク】
ジャイパーカ®医薬品リスク管理計画書 (RMP)
- 感染症
- 出血
- 骨髄抑制
出典
- 日本イーライリリー株式会社. ジャイパーカ錠50mg/ジャイパーカ錠100mg 電子添文 2025年9月改訂第3版
- 日本新薬株式会社. ジャイパーカ錠 適正使用ガイド 2025年9月改訂
- J Clin Oncol. 2025;43(22):2538-2549.
- N Engl J Med. 2023:389:33-44.
最終更新 : 2025年9月22日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。




