Fedratinib
フェドラチニブ (インレビック®)
Fedratinib:フェドラチニブ(インレビック®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1回400mg 1日1回 経口 | 1~ | Day 1~ |
前投薬
その他
| 投与中は1日100mg以上を目安にビタミンB₁経口剤を併用。 |
2025年6月24日、 「骨髄線維症」 を対象として正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヤヌスキナーゼ (JAK) 阻害剤 フェドラチニブ
投与スケジュール
【1コース】連日内服投与
【催吐性】 中等度~高度 (嘔吐頻度≧30%) *
【FN発症】未報告
*NCCN Guidelines Version 2.2025 Antiemesisを引用
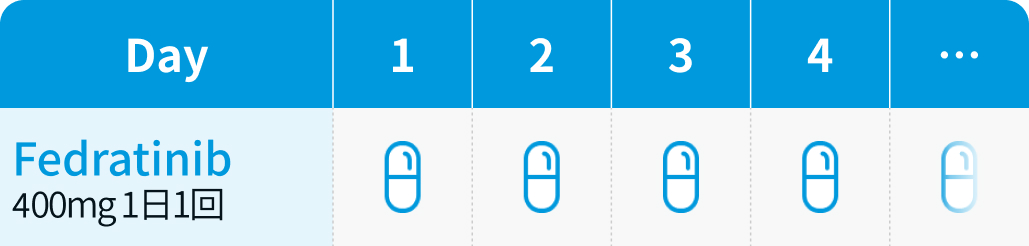
フェドラチニブ1回400mgを1日1回経口投与
ウェルニッケ脳症予防のため、 治療開始前にビタミンB₁濃度を測定し、 不足があれば補充し、 濃度が回復するまで投与を開始しない。 投与中は1日100mg以上を目安にビタミンB₁経口剤を併用し、 必要に応じて濃度を再評価する。 神経学的症状出現時は神経内科と連携の上、 慎重に対応する。
Key Data|臨床試験結果
📊 JAKARTA試験
JAMA Oncol. 2015;1(5):643-651.
中間-II又は高リスクの原発性骨髄線維症、 真性多血症後骨髄線維症、 本態性血小板血症後骨髄線維症の成人患者289例を対象とした、 第III相無作為化比較試験。 患者は、 フェドラチニブ400mg又は500mgを1日1回経口投与する群、 あるいはプラセボ群に無作為に割り付けられ、 少なくとも6サイクル治療を継続した。 主要評価項目は、 24週時点における脾臓体積のベースラインからの35%以上の減少であり、 この効果は4週間後に再確認された。
【有効性】
フェドラチニブ400mg群 (vs プラセボ群)
- 脾臓反応達成率: 36% (vs 1%、 p<0.001)
- 24週時点の症状反応率* : 36% (vs 7%)
*総症状スコアの50%以上の減少
【安全性】主な有害事象: 全Grade (Grade≧3)
フェドラチニブ400mg群
- 貧血 99% (43%)
- 血小板減少症 63% (17%)
- リンパ球減少症 57% (20%)
- 好中球減少症 28% (8%)
- 下痢 66% (5%)
- 嘔吐 42% (3%)
- 悪心 64% (0%)
- 便秘 10% (2%)
- 無力症 9% (2%)
- 腹痛 15% (0%)
- 倦怠感 16% (6%)
- 呼吸困難感 8% (0%)
- 体重減少 4% (0%)
- ALT増加 53% (3%)
- AST増加 60% (2%)
- 高ビリルビン血症 31% (2%)
- クレアチニン増加 54% (3%)
- アミラーゼ増加 26% (2%)
- リパーゼ増加 45% (13%)
フェドラチニブ500mg/日を投与された4例の女性で脳症が報告され、 うち3例ではMRI所見によりウェルニッケ脳症と診断された。
各プロトコル
適格基準
JAKARTA試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0~2
- 好中球数≧1,000/mm³
- 血小板数≧5万/mm³
- 腎機能 : 血清クレアチニン≦1.5×ULN
- 肝機能 : 直接ビリルビン≦2.0×ULN、 AST/ALT≦3× ULN
用量レベル
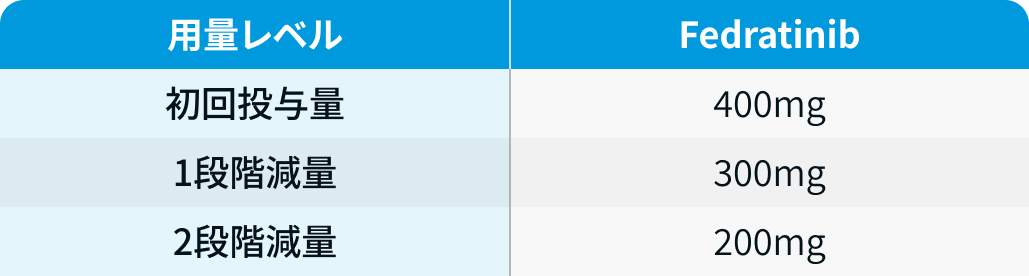
インレビック®電子添文を基に編集部作成
腎障害患者に対する用量調整
CrCl 15mL/min以上、 30mL/min未満の場合は200mgに減量
有害事象発現時の減量・休薬・中止基準

インレビック®電子添文を基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
フェドラチニブはJAK2阻害作用を有する低分子化合物であり、 STATなどの下流分子のリン酸化を抑制することで腫瘍増殖を抑えると考えられている。
🧑⚕️インレビック®は、 JAK2を阻害する骨髄線維症治療薬です。 今後は、 ジャカビ®やオムジャラ®との使い分けについての検討が進むことが期待されます。
東海大学医学部 血液腫瘍内科 扇屋大輔先生
強いCYP3A阻害剤併用時は減量が必要
強いCYP3A阻害剤併用時は200mgに減量し、 併用終了後は300mg→400mgと段階的に増量。
レジメン適用時の注意事項
脳症 : ビタミンB₁欠乏によるウェルニッケ脳症を防ぐため、 投与前にB₁濃度を測定し、 低値なら補充・回復後に開始する。 投与中はB₁経口剤を併用し、 症状があれば必要に応じて再測定する。 嘔吐・下痢による低栄養を避けるため、 制吐剤・止瀉剤の予防投与を検討し、 神経内科と連携して神経症状を観察。
感染症 : 免疫抑制により感染症や日和見感染が発現・増悪することがある。 肝炎ウイルスや結核の再活性化を防ぐため、 投与前に感染の有無を確認し、 必要に応じて処置を行う。 投与中も感染症に注意。
骨髄抑制 : 骨髄抑制があらわれることがあるため、 投与前および投与中は定期的に血液検査を実施し、 状態を観察。
肝機能障害 : 肝機能障害があらわれることがあるため、 投与前および投与中は定期的に肝機能検査を実施。
ぶどう膜炎 : ぶどう膜炎があらわれることがあるため、 眼の異常を定期的に確認し、 異常があれば速やかな受診を指導。
RMP【重要な特定されたリスク】
インレビック®医薬品リスク管理計画書 (RMP)
- 脳症 (ウェルニッケ脳症を含む)
- 骨髄抑制
- 感染症
- 肝機能障害
- ぶどう膜炎
- 出血
- 腎機能障害患者への使用
- CYP3A阻害剤との薬物相互作用
出典
- ブリストル・マイヤーズ スクイブ株式会社 . インレビック®カプセル100mg 電子添文 2025年6月作成 (第1版).
- ブリストル・マイヤーズ スクイブ株式会社 . インレビック®カプセル100mg 適正使用ガイド 2025年6月作成
- JAMA Oncol. 2015;1(5):643-651.
最終更新 : 2025年7月8日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Fedratinib
Fedratinib:フェドラチニブ(インレビック®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1回400mg 1日1回 経口 | 1~ | Day 1~ |
前投薬
その他
| 投与中は1日100mg以上を目安にビタミンB₁経口剤を併用。 |
概要
2025年6月24日、 「骨髄線維症」 を対象として正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヤヌスキナーゼ (JAK) 阻害剤 フェドラチニブ
投与スケジュール
【1コース】連日内服投与
【催吐性】 中等度~高度 (嘔吐頻度≧30%) *
【FN発症】未報告
*NCCN Guidelines Version 2.2025 Antiemesisを引用

フェドラチニブ1回400mgを1日1回経口投与
ウェルニッケ脳症予防のため、 治療開始前にビタミンB₁濃度を測定し、 不足があれば補充し、 濃度が回復するまで投与を開始しない。 投与中は1日100mg以上を目安にビタミンB₁経口剤を併用し、 必要に応じて濃度を再評価する。 神経学的症状出現時は神経内科と連携の上、 慎重に対応する。
Key Data|臨床試験結果
📊 JAKARTA試験
JAMA Oncol. 2015;1(5):643-651.
中間-II又は高リスクの原発性骨髄線維症、 真性多血症後骨髄線維症、 本態性血小板血症後骨髄線維症の成人患者289例を対象とした、 第III相無作為化比較試験。 患者は、 フェドラチニブ400mg又は500mgを1日1回経口投与する群、 あるいはプラセボ群に無作為に割り付けられ、 少なくとも6サイクル治療を継続した。 主要評価項目は、 24週時点における脾臓体積のベースラインからの35%以上の減少であり、 この効果は4週間後に再確認された。
【有効性】
フェドラチニブ400mg群 (vs プラセボ群)
- 脾臓反応達成率: 36% (vs 1%、 p<0.001)
- 24週時点の症状反応率* : 36% (vs 7%)
*総症状スコアの50%以上の減少
【安全性】主な有害事象: 全Grade (Grade≧3)
フェドラチニブ400mg群
- 貧血 99% (43%)
- 血小板減少症 63% (17%)
- リンパ球減少症 57% (20%)
- 好中球減少症 28% (8%)
- 下痢 66% (5%)
- 嘔吐 42% (3%)
- 悪心 64% (0%)
- 便秘 10% (2%)
- 無力症 9% (2%)
- 腹痛 15% (0%)
- 倦怠感 16% (6%)
- 呼吸困難感 8% (0%)
- 体重減少 4% (0%)
- ALT増加 53% (3%)
- AST増加 60% (2%)
- 高ビリルビン血症 31% (2%)
- クレアチニン増加 54% (3%)
- アミラーゼ増加 26% (2%)
- リパーゼ増加 45% (13%)
フェドラチニブ500mg/日を投与された4例の女性で脳症が報告され、 うち3例ではMRI所見によりウェルニッケ脳症と診断された。
各プロトコル
適格基準
JAKARTA試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0~2
- 好中球数≧1,000/mm³
- 血小板数≧5万/mm³
- 腎機能 : 血清クレアチニン≦1.5×ULN
- 肝機能 : 直接ビリルビン≦2.0×ULN、 AST/ALT≦3× ULN
用量レベル

インレビック®電子添文を基に編集部作成
腎障害患者に対する用量調整
CrCl 15mL/min以上、 30mL/min未満の場合は200mgに減量
有害事象発現時の減量・休薬・中止基準

インレビック®電子添文を基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
フェドラチニブはJAK2阻害作用を有する低分子化合物であり、 STATなどの下流分子のリン酸化を抑制することで腫瘍増殖を抑えると考えられている。
🧑⚕️インレビック®は、 JAK2を阻害する骨髄線維症治療薬です。 今後は、 ジャカビ®やオムジャラ®との使い分けについての検討が進むことが期待されます。
東海大学医学部 血液腫瘍内科 扇屋大輔先生
強いCYP3A阻害剤併用時は減量が必要
強いCYP3A阻害剤併用時は200mgに減量し、 併用終了後は300mg→400mgと段階的に増量。
レジメン適用時の注意事項
脳症 : ビタミンB₁欠乏によるウェルニッケ脳症を防ぐため、 投与前にB₁濃度を測定し、 低値なら補充・回復後に開始する。 投与中はB₁経口剤を併用し、 症状があれば必要に応じて再測定する。 嘔吐・下痢による低栄養を避けるため、 制吐剤・止瀉剤の予防投与を検討し、 神経内科と連携して神経症状を観察。
感染症 : 免疫抑制により感染症や日和見感染が発現・増悪することがある。 肝炎ウイルスや結核の再活性化を防ぐため、 投与前に感染の有無を確認し、 必要に応じて処置を行う。 投与中も感染症に注意。
骨髄抑制 : 骨髄抑制があらわれることがあるため、 投与前および投与中は定期的に血液検査を実施し、 状態を観察。
肝機能障害 : 肝機能障害があらわれることがあるため、 投与前および投与中は定期的に肝機能検査を実施。
ぶどう膜炎 : ぶどう膜炎があらわれることがあるため、 眼の異常を定期的に確認し、 異常があれば速やかな受診を指導。
RMP【重要な特定されたリスク】
インレビック®医薬品リスク管理計画書 (RMP)
- 脳症 (ウェルニッケ脳症を含む)
- 骨髄抑制
- 感染症
- 肝機能障害
- ぶどう膜炎
- 出血
- 腎機能障害患者への使用
- CYP3A阻害剤との薬物相互作用
出典
- ブリストル・マイヤーズ スクイブ株式会社 . インレビック®カプセル100mg 電子添文 2025年6月作成 (第1版).
- ブリストル・マイヤーズ スクイブ株式会社 . インレビック®カプセル100mg 適正使用ガイド 2025年6月作成
- JAMA Oncol. 2015;1(5):643-651.
最終更新 : 2025年7月8日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。




