BelaVd
ベランタマブ マホドチン+ボルテゾミブ+デキサメタゾン
Bela:ベランタマブ マホドチン(ブーレンレップ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2.5mg/kg 点滴静注 | 1~ | Day 1 |
BOR:ボルテゾミブ(ベルケイド®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.3mg/kg 皮下投与 | 1~8 | Day 1, 4, 8, 11 |
DEX:デキサメタゾン(レナデックス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 20mg 経口又は静脈内投与 | 1~8 | Day 1, 2, 4, 5, 8, 9, 11, 12 |
前投薬
その他
| デキサメタゾンは、75歳超、BMI<18.5kg/m²、糖質コルチコイドに関連する許容できない副作用の既往がある場合、または開始用量に忍容性がない場合は10mgに減量。 |
| 治療開始前に眼科医の診察を行う。初回から4回目までの各投与前は必ず、以降は必要に応じて、視力検査・細隙灯顕微鏡検査を含む眼科検査を実施し、患者の状態を十分に観察する。 |
| 臨床試験では、ボルテゾミブはベランタマブ マホドチン投与終了約1時間後に投与された。 |
| 臨床試験では、Day 1のデキサメタゾンはベランタマブ マホドチン投与前に実施。 |
ブーレンレップ® : 2024年9月17日、 「再発又は難治性の多発性骨髄腫」 を対象として承認申請、 2025年5月19日に正式承認
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*グラクソ・スミスクライン株式会社の外部サイトへ遷移します
- ボルテゾミブ® (添付文書)
- レナデックス® (添付文書)
投与スケジュール
【1コース】21日間
【催吐性】未分類*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025 Antiemesis未記載 (ボルテゾミブは最小度催吐性リスクに分類)
**DREAMM-7試験のFN発生率<1%を基に編集部が分類
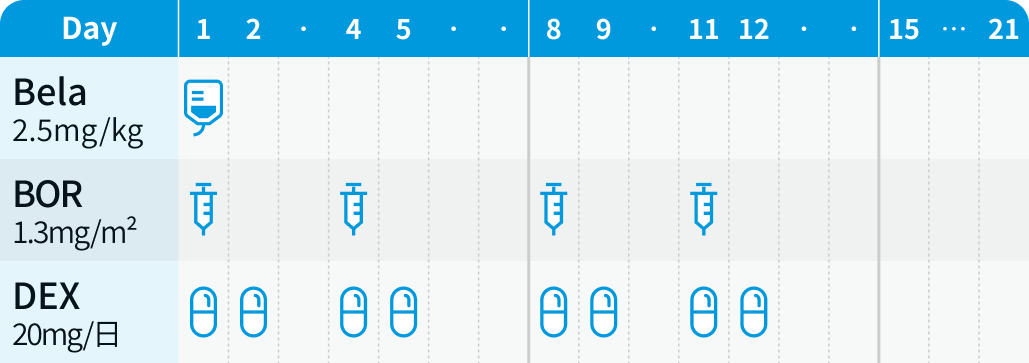
1~8コース目
9コース目以降
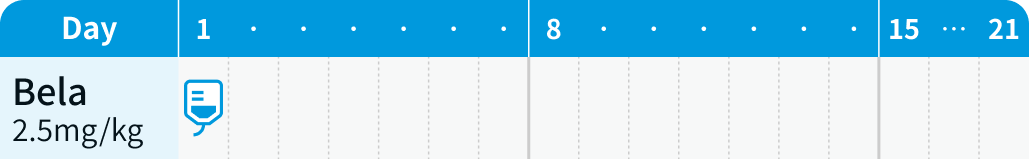
ベランタマブ マホドチン 2.5mg/kgを30分以上かけ3週間間隔で点滴静注
ボルテゾミブ 1~8コースに、 1.3mg/m²をDay 1、 4、 8、 11に皮下投与
デキサメタゾン 1~8コースに、 20mgをDay 1、 2、 4、 5、 8、 9、 11、 12に経口又は静脈内投与
75歳超、 BMI<18.5、 糖質コルチコイドによる重篤な副作用歴、 または開始用量に耐えられない場合、 開始用量10mgに減量可
Key Data|臨床試験結果
📊 DREAMM-7試験
N Engl J Med. 2024;391:393-407.
1レジメン以上の前治療歴を有する再発又は難治性の多発性骨髄腫患者494例を対象とした国際共同の無作為化非盲検第Ⅲ相試験。 ベランタマブ マホドチン、 ボルテゾミブ及びデキサメタゾン併用療法 (BelaVd療法) 群とダラツムマブ、 ボルテゾミブ及びデキサメタゾン併用療法 (DVd療法) 群に無作為に割り付け、 主要評価項目として無増悪生存期間 (PFS) が設定された。
【有効性】BelaVd療法群 (vs DVd群)
- PFS中央値 : 36.6ヵ月 (vs 13.4ヵ月、 ハザード比0.41、 p<0.001)
- 18ヵ月時点の全生存率 : 84% (vs 73%)
- sCRまたはCR以上かつMRD陰性の達成率 : 25% (vs 10%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 貧血 19% (8%)
- 血小板減少症 69% (55%)
- 感染症 70% (31%)
- 肺炎 18% (12%)
- COVID-19 24% (6%)
- 上気道感染 20% (0%)
- 眼障害 79% (34%)
- 霧視 66% (22%)
- ドライアイ 51% (7%)
- 羞明 47% (2%)
- 眼刺激 43% (5%)
- 眼の異物感 44% (3%)
- 眼痛 32% (1%)
- 白内障 20% (7%)
- 下痢 32% (4%)
- 末梢性感覚ニューロパチー 25% (1%)
- 末梢性ニューロパチー 21% (1%)
- 便秘 19% (1%)
- 疲労 19% (4%)
- ALT増加 19% (6%)
- 発熱 19% (<1%)
- 悪心 16% (1%)
- 不眠症 16% (1%)
- AST増加 15% (1%)
- γ-GTP増加 15% (9%)
- Infusion-related reaction 3% (<1%)
- 背部痛 9% (1%)
各プロトコル
適格基準
DREAMM-7試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数 ≧1,500/mm³
- 血小板数 ≧7.5万/mm³
- ヘモグロビン ≧8.0 g/dL
- 腎機能 : eGFR ≧ 30mL/min/1.73m²
- 肝機能 : 総ビリルビン≦1.5 ×ULN、 ALT≦2.5 ×ULN
- 軽度点状角膜症を除く既存の角膜上皮疾患がないこと
用量レベル
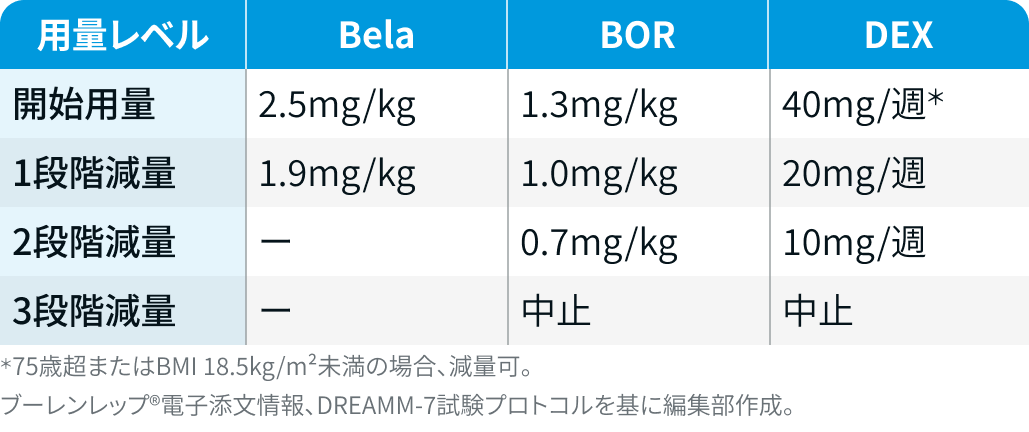
減量・休薬・中止基準
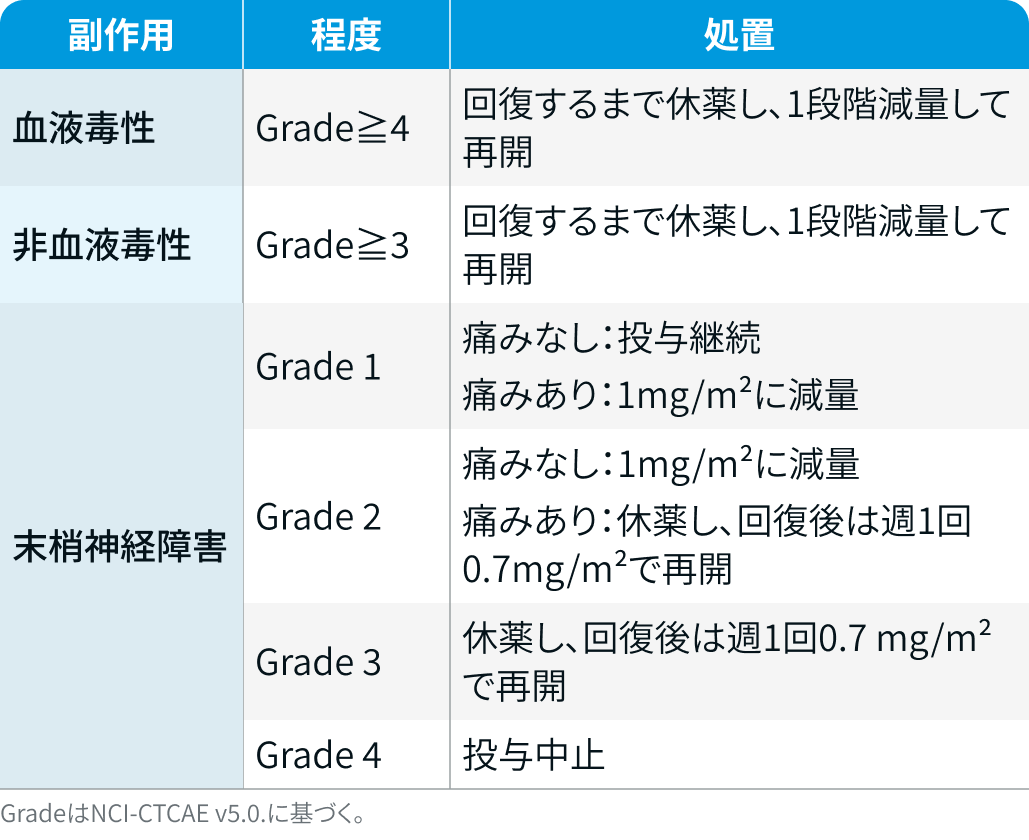
ベランタマブ マホドチン
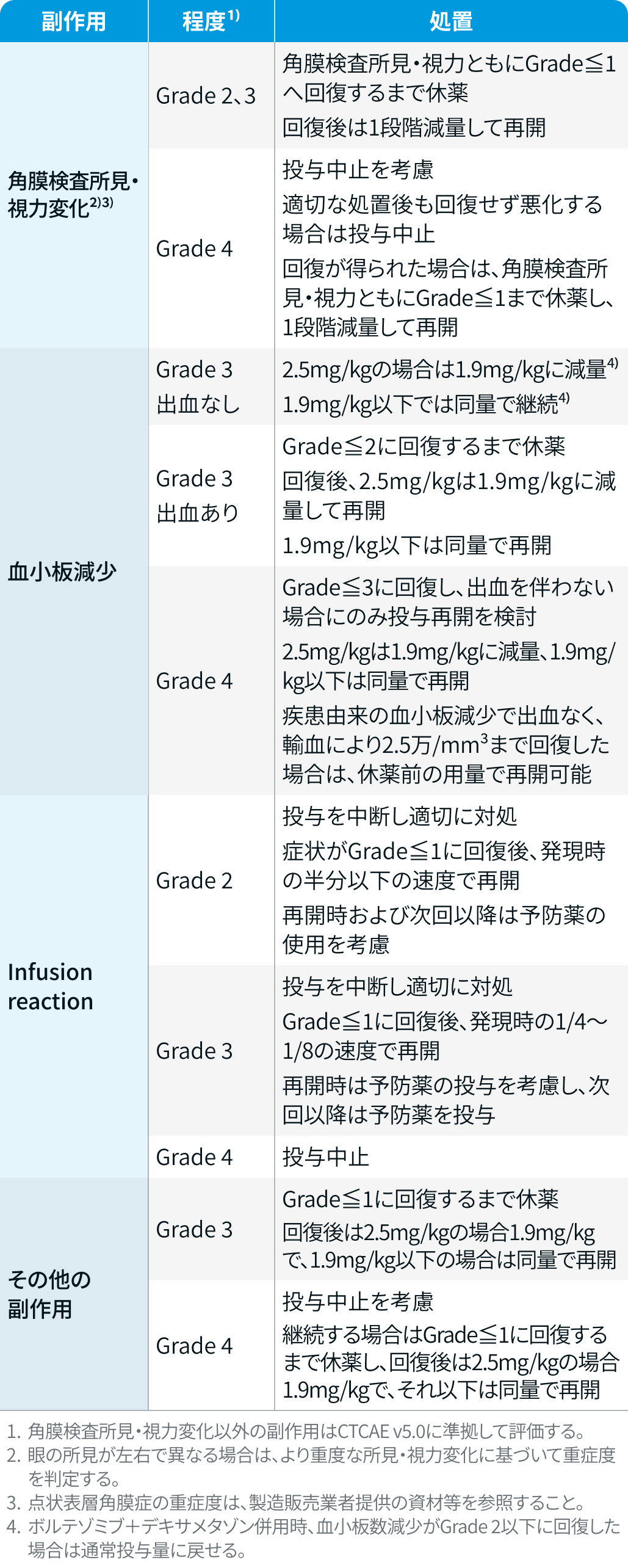
ブーレンレップ®電子添文¹⁾を基に編集部作成
ボルテゾミブ
DREAMM-7試験³⁾のプロトコルを基に編集部作成
眼障害のマネジメント
眼科医師との連携
視力低下を含む眼障害が高頻度にみられることから、 ベランタマブマホドチンの投与に際しては眼科医との連携が不可欠である。 眼科検査の結果は、 休薬や減量の判断に不可欠な情報であるため、 速やかに共有する必要がある。
『ブーレンレップ手帳』や『眼科検査結果記入用紙』を活用し、 検査結果の共有を徹底する。
眼科検査の頻度
初回~4回目までは各投与前に、 以降は必要に応じて視力検査・細隙灯顕微鏡検査を含む眼科的評価を行い、 状態を十分に観察する。
眼障害の評価方法
眼障害の評価は、 角膜検査所見および最高矯正視力の変化に基づいて重症度を判定する。 詳細は『眼科医向けブーレンレップ眼障害マネジメントガイド』を参照。
角膜検査所見の重症度 (KVAスケール) : 軽度の点状表層角膜症 (Grade 1) から角膜上皮欠損 (Grade 4) までの所見に基づき評価される。
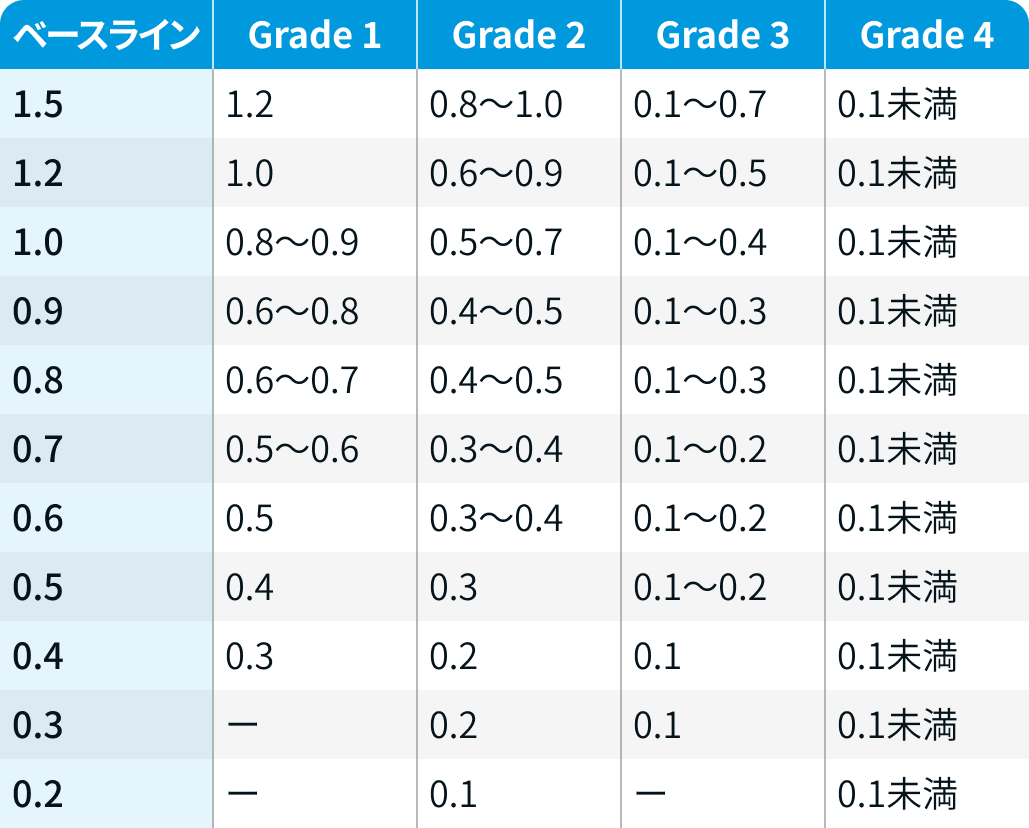
最高矯正視力の変化による重症度 (KVAスケール) : ベースラインの最高矯正視力からの低下の程度により、 Grade 1~4に分類される。
マネジメント
- 眼障害の重症度に応じて、 適切に休薬や減量を行う
- ドライアイなどの眼症状軽減のため、 防腐剤無添加の人工涙液を1日4回以上点眼する
点眼薬の例 : ヒアルロン酸ナトリウムPF点眼液0.1%/0.3% 「日点」、 ヒアレインミニ点眼液0.1%/0.3%、 ソフトサンティアなど
- 治療中はコンタクトレンズの装着を避ける
- 霧視など視力低下を伴う眼障害が高頻度に発現するため、 自動車運転や機械操作時は注意が必要
レジメンの特徴と注意点
作用機序の特徴
ベランタマブ マホドチンは、 BCMAに対するヒト化IgG1抗体に、 微小管重合阻害薬MMAFをペプチドリンカーで結合させた抗体薬物複合体である。 BCMA陽性腫瘍細胞に結合・取り込まれ、 MMAF複合体がアポトーシスを誘導することで抗腫瘍効果を発揮する。 また、 本剤は低フコース化抗体によりADCC・ADCP活性を高め、 Fcγ受容体への結合親和性が強化されている。
レジメン適用時の注意事項
- ポマリドミドおよびデキサメタゾンとの併用療法 (BelaPd) とは用法・用量が異なるため注意する
- 感染症 (特に日和見感染症) の発現や悪化があり得るため、 投与前にニューモシスチス・イロベチイなどの感染有無を確認する
RMP【重要な特定されたリスク】
ブーレンレップ®医薬品リスク管理計画書 (RMP)
- 眼障害
- 血球減少
- 感染症
出典
- グラクソ・スミスクライン株式会社. ブーレンレップ点滴静注用100mg 電子添文 2025年5月 (第1版) [最終確認: 2025/5/29]
- グラクソ・スミスクライン株式会社. ブーレンレップ点滴静注用100mg 適正使用ガイド [最終確認: 2025/5/29]
- N Engl J Med. 2024;391:393-407.
最終更新 : 2025年5月29日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
BelaVd
Bela:ベランタマブ マホドチン(ブーレンレップ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2.5mg/kg 点滴静注 | 1~ | Day 1 |
BOR:ボルテゾミブ(ベルケイド®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.3mg/kg 皮下投与 | 1~8 | Day 1, 4, 8, 11 |
DEX:デキサメタゾン(レナデックス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 20mg 経口又は静脈内投与 | 1~8 | Day 1, 2, 4, 5, 8, 9, 11, 12 |
前投薬
その他
| デキサメタゾンは、75歳超、BMI<18.5kg/m²、糖質コルチコイドに関連する許容できない副作用の既往がある場合、または開始用量に忍容性がない場合は10mgに減量。 |
| 治療開始前に眼科医の診察を行う。初回から4回目までの各投与前は必ず、以降は必要に応じて、視力検査・細隙灯顕微鏡検査を含む眼科検査を実施し、患者の状態を十分に観察する。 |
| 臨床試験では、ボルテゾミブはベランタマブ マホドチン投与終了約1時間後に投与された。 |
| 臨床試験では、Day 1のデキサメタゾンはベランタマブ マホドチン投与前に実施。 |
概要
ブーレンレップ® : 2024年9月17日、 「再発又は難治性の多発性骨髄腫」 を対象として承認申請、 2025年5月19日に正式承認
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*グラクソ・スミスクライン株式会社の外部サイトへ遷移します
- ボルテゾミブ® (添付文書)
- レナデックス® (添付文書)
投与スケジュール
【1コース】21日間
【催吐性】未分類*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025 Antiemesis未記載 (ボルテゾミブは最小度催吐性リスクに分類)
**DREAMM-7試験のFN発生率<1%を基に編集部が分類
1~8コース目

9コース目以降

ベランタマブ マホドチン 2.5mg/kgを30分以上かけ3週間間隔で点滴静注
ボルテゾミブ 1~8コースに、 1.3mg/m²をDay 1、 4、 8、 11に皮下投与
デキサメタゾン 1~8コースに、 20mgをDay 1、 2、 4、 5、 8、 9、 11、 12に経口又は静脈内投与
75歳超、 BMI<18.5、 糖質コルチコイドによる重篤な副作用歴、 または開始用量に耐えられない場合、 開始用量10mgに減量可
Key Data|臨床試験結果
📊 DREAMM-7試験
N Engl J Med. 2024;391:393-407.
1レジメン以上の前治療歴を有する再発又は難治性の多発性骨髄腫患者494例を対象とした国際共同の無作為化非盲検第Ⅲ相試験。 ベランタマブ マホドチン、 ボルテゾミブ及びデキサメタゾン併用療法 (BelaVd療法) 群とダラツムマブ、 ボルテゾミブ及びデキサメタゾン併用療法 (DVd療法) 群に無作為に割り付け、 主要評価項目として無増悪生存期間 (PFS) が設定された。
【有効性】BelaVd療法群 (vs DVd群)
- PFS中央値 : 36.6ヵ月 (vs 13.4ヵ月、 ハザード比0.41、 p<0.001)
- 18ヵ月時点の全生存率 : 84% (vs 73%)
- sCRまたはCR以上かつMRD陰性の達成率 : 25% (vs 10%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 貧血 19% (8%)
- 血小板減少症 69% (55%)
- 感染症 70% (31%)
- 肺炎 18% (12%)
- COVID-19 24% (6%)
- 上気道感染 20% (0%)
- 眼障害 79% (34%)
- 霧視 66% (22%)
- ドライアイ 51% (7%)
- 羞明 47% (2%)
- 眼刺激 43% (5%)
- 眼の異物感 44% (3%)
- 眼痛 32% (1%)
- 白内障 20% (7%)
- 下痢 32% (4%)
- 末梢性感覚ニューロパチー 25% (1%)
- 末梢性ニューロパチー 21% (1%)
- 便秘 19% (1%)
- 疲労 19% (4%)
- ALT増加 19% (6%)
- 発熱 19% (<1%)
- 悪心 16% (1%)
- 不眠症 16% (1%)
- AST増加 15% (1%)
- γ-GTP増加 15% (9%)
- Infusion-related reaction 3% (<1%)
- 背部痛 9% (1%)
各プロトコル
適格基準
DREAMM-7試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数 ≧1,500/mm³
- 血小板数 ≧7.5万/mm³
- ヘモグロビン ≧8.0 g/dL
- 腎機能 : eGFR ≧ 30mL/min/1.73m²
- 肝機能 : 総ビリルビン≦1.5 ×ULN、 ALT≦2.5 ×ULN
- 軽度点状角膜症を除く既存の角膜上皮疾患がないこと
用量レベル

減量・休薬・中止基準
ベランタマブ マホドチン

ブーレンレップ®電子添文¹⁾を基に編集部作成
ボルテゾミブ

DREAMM-7試験³⁾のプロトコルを基に編集部作成
眼障害のマネジメント
眼科医師との連携
視力低下を含む眼障害が高頻度にみられることから、 ベランタマブマホドチンの投与に際しては眼科医との連携が不可欠である。 眼科検査の結果は、 休薬や減量の判断に不可欠な情報であるため、 速やかに共有する必要がある。
『ブーレンレップ手帳』や『眼科検査結果記入用紙』を活用し、 検査結果の共有を徹底する。
眼科検査の頻度
初回~4回目までは各投与前に、 以降は必要に応じて視力検査・細隙灯顕微鏡検査を含む眼科的評価を行い、 状態を十分に観察する。
眼障害の評価方法
眼障害の評価は、 角膜検査所見および最高矯正視力の変化に基づいて重症度を判定する。 詳細は『眼科医向けブーレンレップ眼障害マネジメントガイド』を参照。
角膜検査所見の重症度 (KVAスケール) : 軽度の点状表層角膜症 (Grade 1) から角膜上皮欠損 (Grade 4) までの所見に基づき評価される。
最高矯正視力の変化による重症度 (KVAスケール) : ベースラインの最高矯正視力からの低下の程度により、 Grade 1~4に分類される。

マネジメント
- 眼障害の重症度に応じて、 適切に休薬や減量を行う
- ドライアイなどの眼症状軽減のため、 防腐剤無添加の人工涙液を1日4回以上点眼する
点眼薬の例 : ヒアルロン酸ナトリウムPF点眼液0.1%/0.3% 「日点」、 ヒアレインミニ点眼液0.1%/0.3%、 ソフトサンティアなど
- 治療中はコンタクトレンズの装着を避ける
- 霧視など視力低下を伴う眼障害が高頻度に発現するため、 自動車運転や機械操作時は注意が必要
レジメンの特徴と注意点
作用機序の特徴
ベランタマブ マホドチンは、 BCMAに対するヒト化IgG1抗体に、 微小管重合阻害薬MMAFをペプチドリンカーで結合させた抗体薬物複合体である。 BCMA陽性腫瘍細胞に結合・取り込まれ、 MMAF複合体がアポトーシスを誘導することで抗腫瘍効果を発揮する。 また、 本剤は低フコース化抗体によりADCC・ADCP活性を高め、 Fcγ受容体への結合親和性が強化されている。
レジメン適用時の注意事項
- ポマリドミドおよびデキサメタゾンとの併用療法 (BelaPd) とは用法・用量が異なるため注意する
- 感染症 (特に日和見感染症) の発現や悪化があり得るため、 投与前にニューモシスチス・イロベチイなどの感染有無を確認する
RMP【重要な特定されたリスク】
ブーレンレップ®医薬品リスク管理計画書 (RMP)
- 眼障害
- 血球減少
- 感染症
出典
- グラクソ・スミスクライン株式会社. ブーレンレップ点滴静注用100mg 電子添文 2025年5月 (第1版) [最終確認: 2025/5/29]
- グラクソ・スミスクライン株式会社. ブーレンレップ点滴静注用100mg 適正使用ガイド [最終確認: 2025/5/29]
- N Engl J Med. 2024;391:393-407.
最終更新 : 2025年5月29日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。





