Romiplostim (AA)
ロミプロスチム(ロミプレート®)
Romiplostim:ロミプロスチム(ロミプレート®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 10µg/kg | 1- | Day 1、 8、 15、・・・ |
前投薬
| なし |
その他
| 再生不良性貧血に対する初回投与量は10μg/kgを週1回皮下投与. |
| 用量は5µg/kgずつ増減. |
| 最高投与量は週1回20µg/kg |
| 用量調節の詳細は概要を参照. |
本コンテンツは特定の治療法を推奨するものではございません.個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
トロンボポエチン (TPO) 受容体作動薬 ロミプロスチム
主な有害事象
主な有害事象
*国際共同第Ⅱ/Ⅲ相試験より引用.
- 頭痛 (16.7%)
- 筋痙縮 (16.7%)
- アラニンアミノトランスフェラーゼ増加 (8.3%)
- フィブリンDダイマー増加 (8.3%)
- 倦怠感 (8.3%)
- 四肢痛 (8.3%)
その他重要な有害事象
*添付文書より引用
- 血栓症・血栓塞栓症
- 肺塞栓症 (0.8%)
- 深部静脈血栓症 (0.8%)
- 心筋梗塞 (0.6%)
- 血栓性静脈炎 (0.5%)
- 骨髄レチクリン増生 (1.6%)
特徴と注意点
作用機序
- トロンボポエチン受容体結合配列とヒトIgG1のFc領域を併せ持つ遺伝子組み換え融合タンパク質.
- トロンボポエチン受容体を介して、 巨核球とその前駆細胞、 造血幹細胞や造血前駆細胞に作用する.
① 巨核球による血小板造血作用、 及び 巨核球系前駆細胞の増殖や分化を促進し、 血小板を増加させる.
② 造血幹細胞及び造血前駆細胞の増殖や分化を促進し、 血小板だけでなく赤血球及び好中球を増加させる.
適応
- 適応 : 再生不良性貧血 (AA)、 及び慢性特発性血小板減少性紫斑病 (cITP).
AA : aplastic anemia cITP : chronic idiopathic thrombocytopenic purpura ※近年、 免疫性血小板減少性紫斑病 (immune thrombocytopenic purpura)とも呼ばれる.
- AAにおいては、 以下の場合に使用可能.
① シクロスポリン又は抗胸腺細胞免疫グロブリンで未治療の場合は、 原則として両剤と併用する.
② シクロスポリンのみとの併用は、 抗胸腺細胞免疫グロブリンが適用できない場合に考慮.
- AAは重症度によって予後や治療方針が大きく異なるため、 臨床成績の内容を熟知し、 有効性及び安全性を十分に理解した上で、 最新の再生不良性貧血の参照ガイドを参考に、 本剤の投与が適切と判断される患者に投与.
用法・用量
- AAとcITPで用法及び用量が異なる.
- 以下はAAにおける用法・用量・用量調節について記載する.
【Romiplostimの用法・用量】
- 初回投与量10μg/kgを週1回皮下投与.
- 用量は通常5µg/kgずつ増減.
- 最高投与量は20μg/kg.
- 下記を参照の上、 治療上必要最小限の用量で使用する.
【Romiplostimの用量調節】
血小板数に応じた用量調節
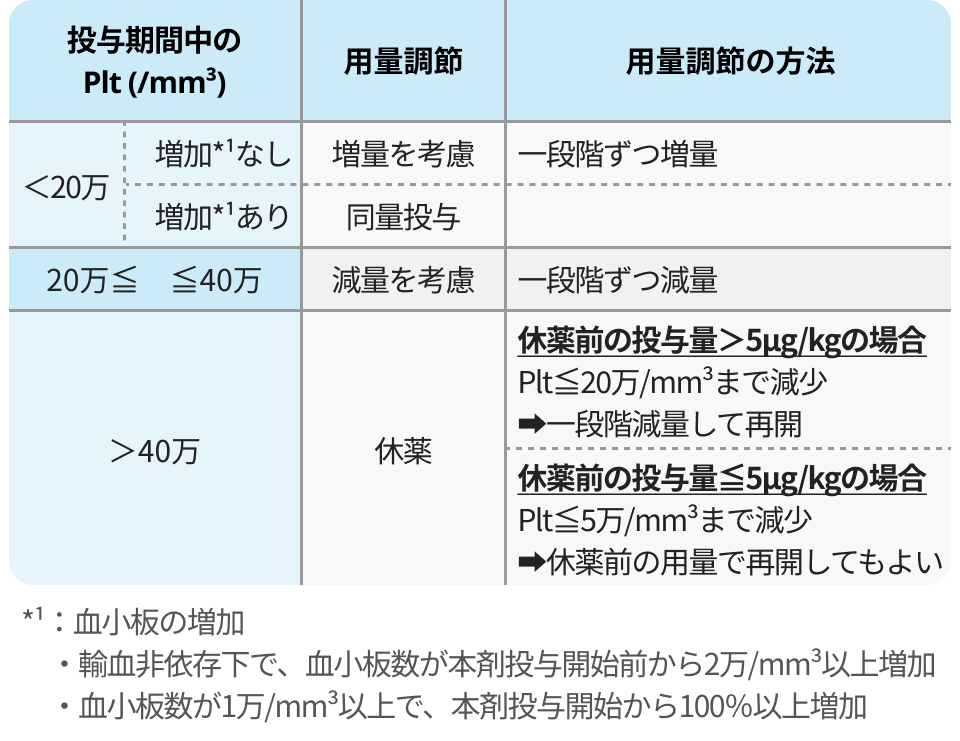
3血球系統に応じた用量調整
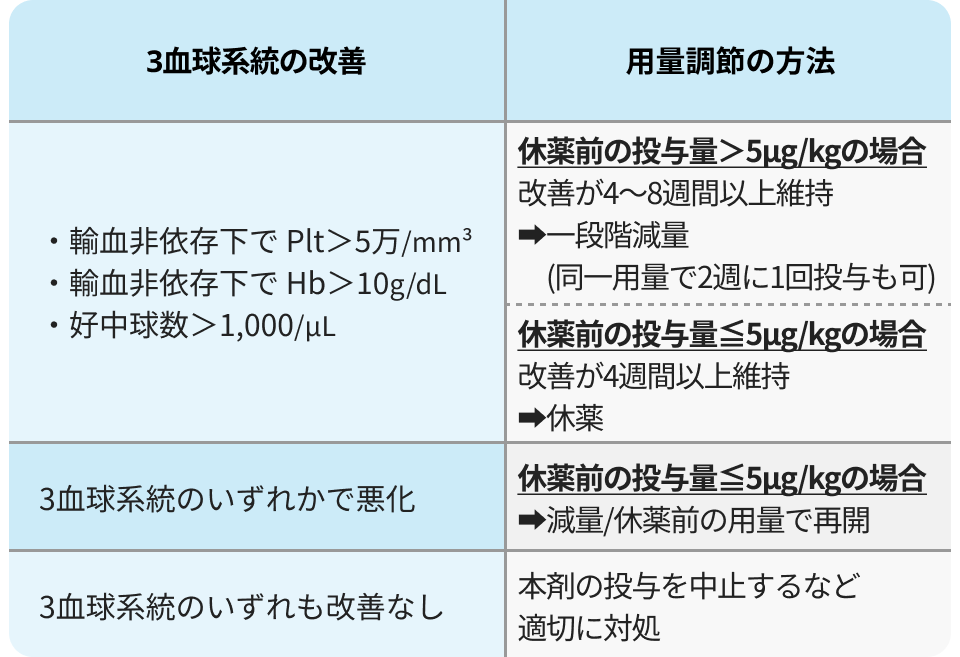
重大な有害事象とその対策
血栓症・血栓塞栓症
- 肺塞栓症 (0.8%)、 深部静脈血栓症 (0.8%)、 心筋梗塞 (0.6%)、 血栓性静脈炎 (0.5%) 等があらわれることがある.
- 一般に血小板数が正常範囲の上限 (400,000/μL)を超えると血栓症又は血栓塞栓症のリスクが増大する.
- 発現頻度は、 cITPの承認時までの臨床試験に基づく.
骨髄レチクリン増生
- 骨髄線維化があらわれる可能性がある.
- 血球系の形態異常又は血球減少を認めた場合は、 本剤の投与を中止する.
- 線維化状態の確認のため骨髄生検・特殊染色等の実施を考慮する.
臨床試験
531-002試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験.
- 対象 : 免疫抑制療法に不応又は免疫抑制療法が適用とならない血小板減少症を有するAA患者31例.
- 主要評価項目 : 投与27週時における血液学的反応率.
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.
- 結果 : 血液学的反応(血小板反応、 赤血球反応、 好中球反応のいずれか) が認められた被験者は、 31例中26例(83.9%、 95%CI:66.3, 94.5)だった.
531-003試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験
- 対象 : 免疫抑制療法未治療のAA患者17例.
- 主要評価項目 : 投与27週時における効果判定基準に基づくCR又はPRを示した被験者の割合.
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.ATG及びCsAと併用投与.
ATG : 抗ヒト胸腺細胞免疫グロブリン CsA : シクロスポリンA
- 結果 : CR又はPRを達成した被験者は17例中13例 (76.5%、 95%CI: 50.10, 93.19).
531-004試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験.
- 対象 : 免疫抑制療法未治療のAA患者24例.
- 主要評価項目 : 投与27週時における効果判定基準に基づくCR又はPRを示した被験者の割合
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.CsAと併用投与
- 結果 : CR又はPRを達成した被験者は24例中10例(41.7%、 95%CI: 22.11、 63.36).
参考文献
関連コンテンツ
HOKUTO表・計算ツール
HOKUTO表・計算ツール
最終更新 : 2024年2月7日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Romiplostim (AA)
Romiplostim:ロミプロスチム(ロミプレート®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 10µg/kg | 1- | Day 1、 8、 15、・・・ |
前投薬
| なし |
その他
| 再生不良性貧血に対する初回投与量は10μg/kgを週1回皮下投与. |
| 用量は5µg/kgずつ増減. |
| 最高投与量は週1回20µg/kg |
| 用量調節の詳細は概要を参照. |
概要
本コンテンツは特定の治療法を推奨するものではございません.個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
トロンボポエチン (TPO) 受容体作動薬 ロミプロスチム
主な有害事象
主な有害事象
*国際共同第Ⅱ/Ⅲ相試験より引用.
- 頭痛 (16.7%)
- 筋痙縮 (16.7%)
- アラニンアミノトランスフェラーゼ増加 (8.3%)
- フィブリンDダイマー増加 (8.3%)
- 倦怠感 (8.3%)
- 四肢痛 (8.3%)
その他重要な有害事象
*添付文書より引用
- 血栓症・血栓塞栓症
- 肺塞栓症 (0.8%)
- 深部静脈血栓症 (0.8%)
- 心筋梗塞 (0.6%)
- 血栓性静脈炎 (0.5%)
- 骨髄レチクリン増生 (1.6%)
特徴と注意点
作用機序
- トロンボポエチン受容体結合配列とヒトIgG1のFc領域を併せ持つ遺伝子組み換え融合タンパク質.
- トロンボポエチン受容体を介して、 巨核球とその前駆細胞、 造血幹細胞や造血前駆細胞に作用する.
① 巨核球による血小板造血作用、 及び 巨核球系前駆細胞の増殖や分化を促進し、 血小板を増加させる.
② 造血幹細胞及び造血前駆細胞の増殖や分化を促進し、 血小板だけでなく赤血球及び好中球を増加させる.
適応
- 適応 : 再生不良性貧血 (AA)、 及び慢性特発性血小板減少性紫斑病 (cITP).
AA : aplastic anemia cITP : chronic idiopathic thrombocytopenic purpura ※近年、 免疫性血小板減少性紫斑病 (immune thrombocytopenic purpura)とも呼ばれる.
- AAにおいては、 以下の場合に使用可能.
① シクロスポリン又は抗胸腺細胞免疫グロブリンで未治療の場合は、 原則として両剤と併用する.
② シクロスポリンのみとの併用は、 抗胸腺細胞免疫グロブリンが適用できない場合に考慮.
- AAは重症度によって予後や治療方針が大きく異なるため、 臨床成績の内容を熟知し、 有効性及び安全性を十分に理解した上で、 最新の再生不良性貧血の参照ガイドを参考に、 本剤の投与が適切と判断される患者に投与.
用法・用量
- AAとcITPで用法及び用量が異なる.
- 以下はAAにおける用法・用量・用量調節について記載する.
【Romiplostimの用法・用量】
- 初回投与量10μg/kgを週1回皮下投与.
- 用量は通常5µg/kgずつ増減.
- 最高投与量は20μg/kg.
- 下記を参照の上、 治療上必要最小限の用量で使用する.
【Romiplostimの用量調節】
血小板数に応じた用量調節

3血球系統に応じた用量調整

重大な有害事象とその対策
血栓症・血栓塞栓症
- 肺塞栓症 (0.8%)、 深部静脈血栓症 (0.8%)、 心筋梗塞 (0.6%)、 血栓性静脈炎 (0.5%) 等があらわれることがある.
- 一般に血小板数が正常範囲の上限 (400,000/μL)を超えると血栓症又は血栓塞栓症のリスクが増大する.
- 発現頻度は、 cITPの承認時までの臨床試験に基づく.
骨髄レチクリン増生
- 骨髄線維化があらわれる可能性がある.
- 血球系の形態異常又は血球減少を認めた場合は、 本剤の投与を中止する.
- 線維化状態の確認のため骨髄生検・特殊染色等の実施を考慮する.
臨床試験
531-002試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験.
- 対象 : 免疫抑制療法に不応又は免疫抑制療法が適用とならない血小板減少症を有するAA患者31例.
- 主要評価項目 : 投与27週時における血液学的反応率.
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.
- 結果 : 血液学的反応(血小板反応、 赤血球反応、 好中球反応のいずれか) が認められた被験者は、 31例中26例(83.9%、 95%CI:66.3, 94.5)だった.
531-003試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験
- 対象 : 免疫抑制療法未治療のAA患者17例.
- 主要評価項目 : 投与27週時における効果判定基準に基づくCR又はPRを示した被験者の割合.
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.ATG及びCsAと併用投与.
ATG : 抗ヒト胸腺細胞免疫グロブリン CsA : シクロスポリンA
- 結果 : CR又はPRを達成した被験者は17例中13例 (76.5%、 95%CI: 50.10, 93.19).
531-004試験 (論文未公表でありインタビューフォームの情報を参照し掲載)
- 国際共同非盲検個体内用量調整試験.
- 対象 : 免疫抑制療法未治療のAA患者24例.
- 主要評価項目 : 投与27週時における効果判定基準に基づくCR又はPRを示した被験者の割合
- 介入 : 10μg/kgで週1回投与を開始し、 血球数等に応じて用量を5~20μg/kgの間で適宜調整.CsAと併用投与
- 結果 : CR又はPRを達成した被験者は24例中10例(41.7%、 95%CI: 22.11、 63.36).
参考文献
関連コンテンツ
HOKUTO表・計算ツール
HOKUTO表・計算ツール
最終更新 : 2024年2月7日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。





