Dabrafenib + Trametinib
ダブラフェニブ + トラメチニブ
Dabrafenib:ダブラフェニブ(タフィンラー®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 150mg 1日2回 経口 (空腹時) | 1~ | day1~ |
Trametinib:トラメチニブ(メキニスト®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2mg 1日1回 経口 (空腹時) | 1~ | day1~ |
その他
| 他の抗悪性腫瘍薬との併用について有効性及び安全性は確立していない. |
| 有害事象発現時の休薬、 減量、 中止基準及び用量調節の目安は概要欄参照. |
| 食事の影響を避けるため食前1時間から食後2時間の服用は避ける. |
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
BRAF阻害薬 ダブラフェニブ
MEK阻害薬 トラメチニブ
*ノバルティス ファーマ株式会社の外部サイトへ遷移します.
主な有害事象
X2201試験¹⁾より引用.
骨髄抑制
- 貧血 (18.2%)
主な有害事象
- 発熱 (76.4%)
- 倦怠感 (52.7%)
- 悪心 (49.1%)
- 悪寒 (56.4%)
- 頭痛 (38.2%)
- 便秘 (43.6%)
- 嘔吐 (25.5%)
- 咳嗽 (54.5%)
- 下痢 (34.5%)
- 発疹 (30.0%)
- AST増加 (38.2%)
- 関節痛 (38.2%)
- 高血糖 (47.3%)
- 末梢浮腫 (49.1%)
- 筋肉痛 (45.5%)
特徴と注意点
特徴
造血器腫瘍に対しては、 BRAF遺伝子変異を有する再発または難治性の有毛細胞白血病に適応を有する.
ダブラフェニブ RAS/RAF/MEK/ERK (MAPK) シグナル伝達経路における変異型BRAF (V600E、 V600KおよびV600D変異陽性) のキナーゼ活性を阻害するBRAF阻害剤である。
MAPK: Mitogen-activated protein kinase、 MEK: Mitogen-activated extracellular signal-regulated kinase
トラメチニブ MAPKシグナル伝達経路におけるMEK1/MEK2の活性化およびキナーゼ活性を阻害するMEK阻害剤である。
腫瘍進行時はMAPKシグナル伝達経路の再活性化が認められ、 RAFのBRAF V600遺伝子変異がBRAF活性を亢進させ、MAPKシグナル伝達経路を恒常的に活性化させると考えられている。
ダブラフェニブとトラメチニブの併用は、 MAPK経路のBRAFとMEKを阻害することでダブラフェニブ単剤に比べ、 腫瘍増殖を阻害または遅延させる。
注意点
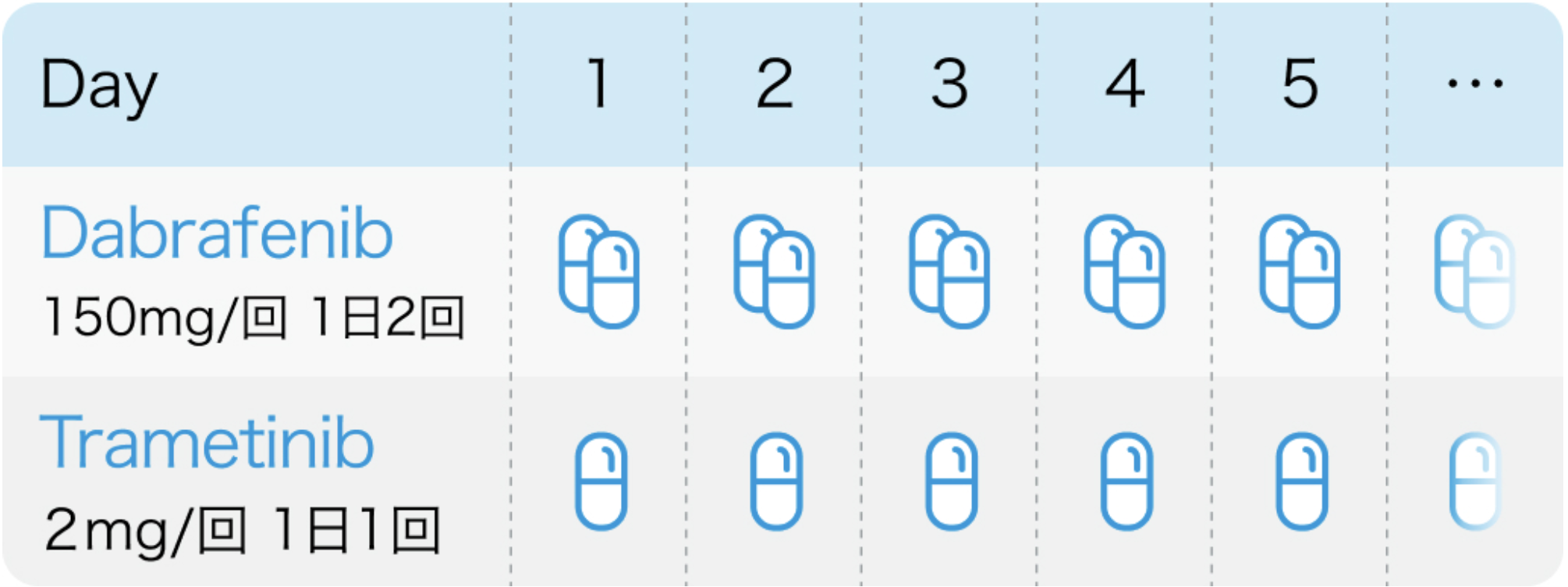
タフィンラー®、メキニスト®添付文書より作図
- 食事の影響を受けるため食事の1時間前から食後2時間までの間の服用は避ける.
- ダブラフェニブとトラメチニブ以外の抗悪性腫瘍剤との併用における有用性および安全性は確立していない.
- 発熱が高頻度に認められる. 38.0℃以上の発熱時はダブラフェニブとトラメチニブをいずれも休薬する.
- 発熱時は感染症等の有無を評価し、 解熱剤で効果不十分な場合は経口ステロイド剤の投与を検討する.
- 解熱後24時間以上発熱がない場合は休薬前と同量で再開する.
- 38.0℃未満の発熱または悪寒、 戦慄、 寝汗、 インフルエンザ用症状等の発熱の初期症状の再発が認められた時点でいずれの薬剤も休薬もしくは減量を検討する.
- 休薬しても4週間以内に発熱がGrade1以下またはベースラインに軽快しない場合は、いずれの薬剤も中止する.
休薬、 減量および中止基準

タフィンラー®、メキニスト®添付文書より作図
用量調節の目安
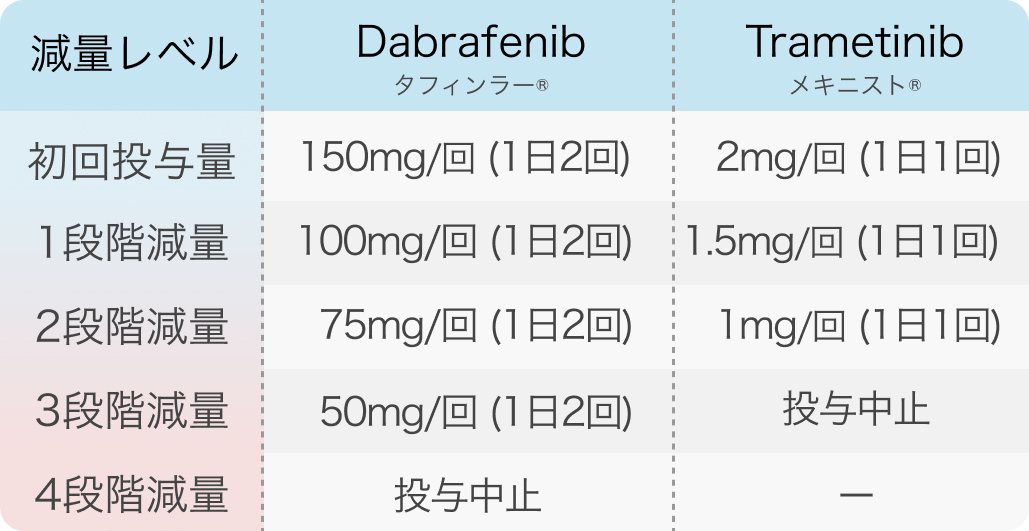
タフィンラー®、メキニスト®添付文書より作図
関連する臨床試験の結果
X2201試験¹⁾
標準的な治療選択肢のないBRAF V600E遺伝子変異を有する悪性腫瘍患者 (206名 うち有毛細胞白血病55名含む)を対象にダブラフェニブ+トラメチニブ併用療法の有効性および安全性を検討した国際共同第II相臨床試験.
結果 (有毛細胞白血病55名)
ORR : 89% (95%CI 77.8-95.9)
- CR with MRD : 18%
- CR without MRD : 47%
DOR中央値 : 未到達
- 6ヵ月DOR率 : 100% (95%CI 100.0-100.0)
- 12ヵ月DOR率 : 97.7% (95%CI 84.9-99.7)
- 24ヵ月DOR率 : 97.9% (95%CI 84.9-99.7)
PFS中央値 : 未到達
- 6ヵ月PFS率 : 96.4% (95%CI 86.2-99.1)
- 12ヵ月PFS率 : 96.4% (95%CI 86.2-99.1)
- 24ヵ月PFS率 : 94.4% (95%CI 83.5-98.1)
OS中央値 : 未到達
- 6ヵ月生存率 : 96.4% (95%CI 86.2-99.1)
- 12ヵ月生存率 : 96.4% (95%CI 86.2-99.1)
- 24ヵ月生存率 : 94.5% (95%CI 83.9-98.2)
安全性 (全被験者206名)
- 重篤な有害事象 : 発熱23例 (11.2%)、 肺炎13例 (6.3%)、 尿路感染8例 (3.9%)、 嘔吐7例 (3.4%)、 敗血症5例 (2.4%)
- 投与中止に至った有害事象 : 悪心3例 (1.5%)、 呼吸困難、 駆出率減少、 頭痛、 胸水、 肺炎、 発熱、 敗血症各2例 (1.0%)
ORR: Overall Response Rate (全奏効率)、 CR: Complete Response (完全奏効)、 MRD: Minimal Residual Disease (微小残存病変)、 DOR: Duration Of Response (奏効期間)、 PFS: Progression Free Survival (無増悪生存)、 OS: Overall Survival (全生存)
出典
1) Nat Med. 2023 May;29(5):1103-1112.
最終更新 : 2025年3月28日
執筆担当 : 北里大学病院薬剤部 宮島律子
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Dabrafenib + Trametinib
Dabrafenib:ダブラフェニブ(タフィンラー®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 150mg 1日2回 経口 (空腹時) | 1~ | day1~ |
Trametinib:トラメチニブ(メキニスト®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2mg 1日1回 経口 (空腹時) | 1~ | day1~ |
その他
| 他の抗悪性腫瘍薬との併用について有効性及び安全性は確立していない. |
| 有害事象発現時の休薬、 減量、 中止基準及び用量調節の目安は概要欄参照. |
| 食事の影響を避けるため食前1時間から食後2時間の服用は避ける. |
概要
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
BRAF阻害薬 ダブラフェニブ
MEK阻害薬 トラメチニブ
*ノバルティス ファーマ株式会社の外部サイトへ遷移します.
主な有害事象
X2201試験¹⁾より引用.
骨髄抑制
- 貧血 (18.2%)
主な有害事象
- 発熱 (76.4%)
- 倦怠感 (52.7%)
- 悪心 (49.1%)
- 悪寒 (56.4%)
- 頭痛 (38.2%)
- 便秘 (43.6%)
- 嘔吐 (25.5%)
- 咳嗽 (54.5%)
- 下痢 (34.5%)
- 発疹 (30.0%)
- AST増加 (38.2%)
- 関節痛 (38.2%)
- 高血糖 (47.3%)
- 末梢浮腫 (49.1%)
- 筋肉痛 (45.5%)
特徴と注意点
特徴
造血器腫瘍に対しては、 BRAF遺伝子変異を有する再発または難治性の有毛細胞白血病に適応を有する.
ダブラフェニブ RAS/RAF/MEK/ERK (MAPK) シグナル伝達経路における変異型BRAF (V600E、 V600KおよびV600D変異陽性) のキナーゼ活性を阻害するBRAF阻害剤である。
MAPK: Mitogen-activated protein kinase、 MEK: Mitogen-activated extracellular signal-regulated kinase
トラメチニブ MAPKシグナル伝達経路におけるMEK1/MEK2の活性化およびキナーゼ活性を阻害するMEK阻害剤である。
腫瘍進行時はMAPKシグナル伝達経路の再活性化が認められ、 RAFのBRAF V600遺伝子変異がBRAF活性を亢進させ、MAPKシグナル伝達経路を恒常的に活性化させると考えられている。
ダブラフェニブとトラメチニブの併用は、 MAPK経路のBRAFとMEKを阻害することでダブラフェニブ単剤に比べ、 腫瘍増殖を阻害または遅延させる。
注意点

タフィンラー®、メキニスト®添付文書より作図
- 食事の影響を受けるため食事の1時間前から食後2時間までの間の服用は避ける.
- ダブラフェニブとトラメチニブ以外の抗悪性腫瘍剤との併用における有用性および安全性は確立していない.
- 発熱が高頻度に認められる. 38.0℃以上の発熱時はダブラフェニブとトラメチニブをいずれも休薬する.
- 発熱時は感染症等の有無を評価し、 解熱剤で効果不十分な場合は経口ステロイド剤の投与を検討する.
- 解熱後24時間以上発熱がない場合は休薬前と同量で再開する.
- 38.0℃未満の発熱または悪寒、 戦慄、 寝汗、 インフルエンザ用症状等の発熱の初期症状の再発が認められた時点でいずれの薬剤も休薬もしくは減量を検討する.
- 休薬しても4週間以内に発熱がGrade1以下またはベースラインに軽快しない場合は、いずれの薬剤も中止する.
休薬、 減量および中止基準

タフィンラー®、メキニスト®添付文書より作図
用量調節の目安

タフィンラー®、メキニスト®添付文書より作図
関連する臨床試験の結果
X2201試験¹⁾
標準的な治療選択肢のないBRAF V600E遺伝子変異を有する悪性腫瘍患者 (206名 うち有毛細胞白血病55名含む)を対象にダブラフェニブ+トラメチニブ併用療法の有効性および安全性を検討した国際共同第II相臨床試験.
結果 (有毛細胞白血病55名)
ORR : 89% (95%CI 77.8-95.9)
- CR with MRD : 18%
- CR without MRD : 47%
DOR中央値 : 未到達
- 6ヵ月DOR率 : 100% (95%CI 100.0-100.0)
- 12ヵ月DOR率 : 97.7% (95%CI 84.9-99.7)
- 24ヵ月DOR率 : 97.9% (95%CI 84.9-99.7)
PFS中央値 : 未到達
- 6ヵ月PFS率 : 96.4% (95%CI 86.2-99.1)
- 12ヵ月PFS率 : 96.4% (95%CI 86.2-99.1)
- 24ヵ月PFS率 : 94.4% (95%CI 83.5-98.1)
OS中央値 : 未到達
- 6ヵ月生存率 : 96.4% (95%CI 86.2-99.1)
- 12ヵ月生存率 : 96.4% (95%CI 86.2-99.1)
- 24ヵ月生存率 : 94.5% (95%CI 83.9-98.2)
安全性 (全被験者206名)
- 重篤な有害事象 : 発熱23例 (11.2%)、 肺炎13例 (6.3%)、 尿路感染8例 (3.9%)、 嘔吐7例 (3.4%)、 敗血症5例 (2.4%)
- 投与中止に至った有害事象 : 悪心3例 (1.5%)、 呼吸困難、 駆出率減少、 頭痛、 胸水、 肺炎、 発熱、 敗血症各2例 (1.0%)
ORR: Overall Response Rate (全奏効率)、 CR: Complete Response (完全奏効)、 MRD: Minimal Residual Disease (微小残存病変)、 DOR: Duration Of Response (奏効期間)、 PFS: Progression Free Survival (無増悪生存)、 OS: Overall Survival (全生存)
出典
1) Nat Med. 2023 May;29(5):1103-1112.
最終更新 : 2025年3月28日
執筆担当 : 北里大学病院薬剤部 宮島律子
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。





