Marstacimab
マルスタシマブ(ヒムペブジ®)
Marstacimab:マルスタシマブ(ヒムペブジ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 300mg 皮下注射 | ー | Day 1 |
| 150mg 皮下注射 | ー | Day 8、15… |
前投薬
その他
| 体重50kg以上で効果不十分な場合は、週1回300mgへの増量投与が可能 |
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
抗TFPIモノクローナル抗体 マルスタシマブ
*ファイザー株式会社の外部サイトへ遷移します
投与スケジュール
血液凝固第Ⅷ因子又は第Ⅸ因子に対するインヒビターを保有しない先天性血友病患者における出血傾向の抑制

通常、 12歳以上かつ体重35kg以上の患者には、 Marstacimab (遺伝子組換え) として初回に300mgを皮下投与し、 以降は1週間隔で1回150mgを皮下投与する。 なお、 体重50kg以上で効果不十分な場合には、 1週間隔で1回300mgに増量して皮下投与できる。
ヒムペブジ皮下注150mgペン 添付文書¹⁾より引用
Key Data|臨床試験結果
📊 B7841005試験
ヒムペブジ皮下注150mgペン 添付文書¹⁾よりデータ引用
インヒビター非保有の中等症~重症血友病AまたはB患者を対象に、 Marstacimab皮下投与の有効性を、 出血時補充療法または定期補充療法を行っていた観察期間 (6ヵ月) とMarstacimab投与期間 (12ヵ月) の年換算出血率 (ABR) を比較して評価した。
【有効性】
年換算出血率 (ABR) 最小二乗平均値
● 導入前に出血時補充療法を受けた群 (33例)
- 導入前 [観察期間] : 39.86 回/年
- 導入後 [投与期間] : 3.20 回/年
● 導入前に定期補充療法を受けた群 (83例)
- 導入前 [観察期間] : 7.90 回/年
- 導入後 [投与期間] : 5.09 回/年
【安全性】
- 注射部位そう痒感 3.4%
- そう痒症 3.4%
- プロトロンビンフラグメント1・2増加 2.6%
- 注射部位紅斑 2.6%
特徴と注意点
🧑⚕️ヒムペブジ®は、 外因系血液凝固反応の主要な制御因子であるTFPIを阻害し、 外因系経路を増強することで、 血友病AおよびBの両方に有効な新規作用機序の薬剤です。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序
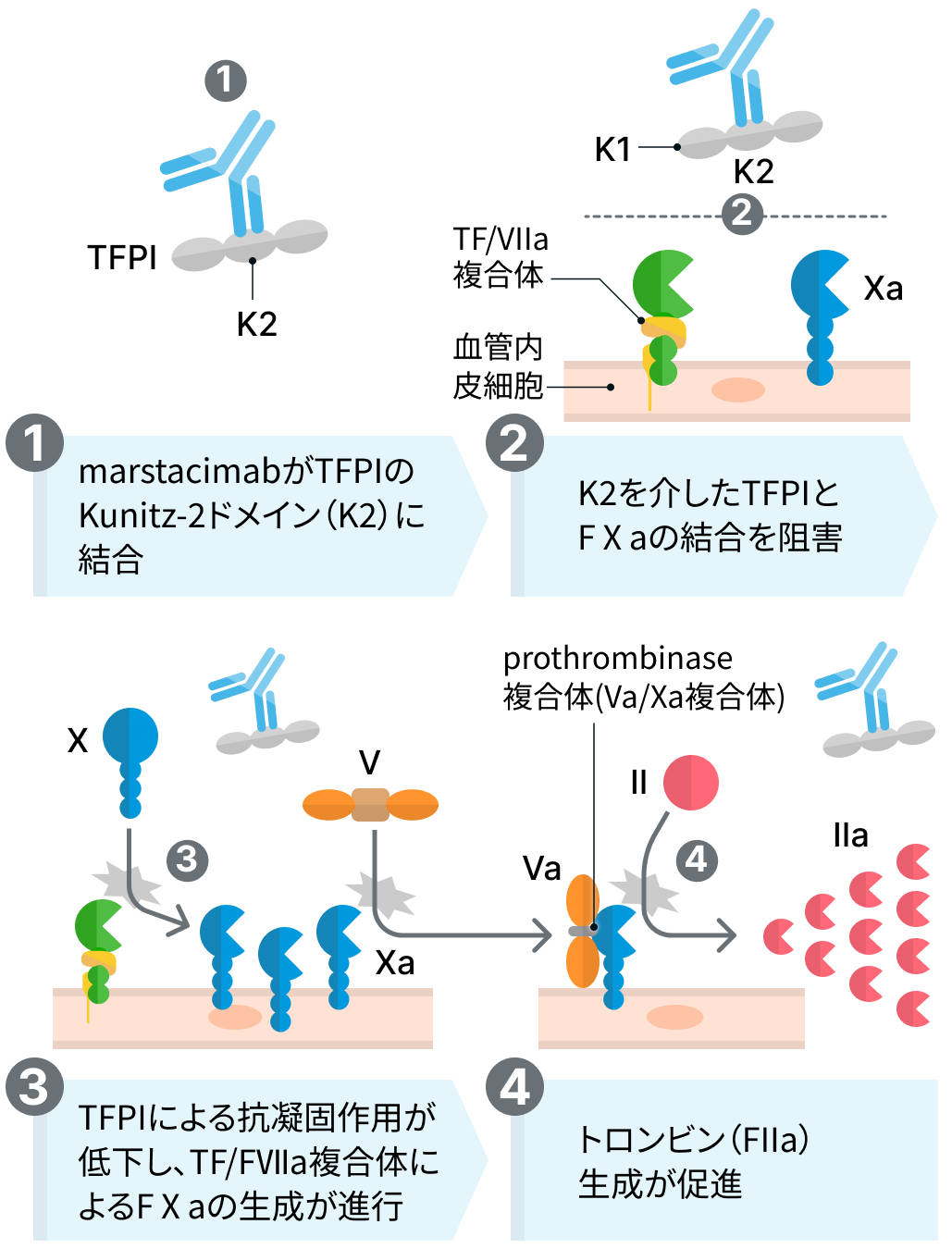
編集部作図
Marstacimabは、 組織因子経路インヒビター (TFPI) のKunitzドメイン2 (K2) を標的とするヒトモノクローナルIgG1抗体である。 TFPIはK2を介して活性型血液凝固第X因子に結合しこれを阻害するが、 MarstacimabはTFPIによるこの活性型第X因子の阻害を抑制することで、 外因系凝固経路を増強する。
適用時の注意事項
- 出血傾向の抑制を目的とした定期投与専用であり、 出血時の止血には使用しない
- 血液凝固第VIII因子または第IX因子製剤から切り替える際は、 前治療薬の半減期を考慮し、 適切な時期に中止する
- 非血液凝固因子製剤から切り替える際は、 前治療薬の半減期に基づき、 少なくとも半減期の5倍以上の休薬期間を設け、 必要に応じて凝固因子製剤による補充療法を行う
使用が想定される各血液凝固因子製剤および非血液凝固因子製剤の半減期については、 『ヒムペブジ®皮下注150mgペン 投与中の注意事項』の6~7ページに記載されている。
- 自己注射は、 十分な教育と訓練を実施し、 患者または介護者が確実に投与できることを確認したうえで、 医師の管理・指導のもとで実施する
- 本剤は冷蔵庫から出して直射日光を避けながら外箱のまま15~30分かけて自然に室温 (30℃以下) に戻す。 電子レンジや熱湯で温めないこと。 室温に戻した薬剤は再冷蔵せず、 7日以内に使用する。 振とうは避ける
- 注射部位は腹部または大腿前面から選択する。 腹部に投与する場合は、 座位で前かがみになり腹部をゆるめた姿勢で、 臍部から5cm以上離れた部位を選ぶ。 大腿前面に投与する場合も座位で行い、 毎回注射部位を変更することが望ましい。 300mgを投与する場合は、 150mgずつを2カ所の異なる部位に分けて投与する。
投与を忘れた場合の対応
投与予定日に投与できなかった場合は、 可能な限り速やかに予定用量で再開し、 以降は原則としてその日を起点に週1回の投与を継続する。
再開日が最終投与日から14日以上経過している場合は、 再開時の初回投与量を300mgとする (300mgで治療中の患者が14日以上投与を空けた場合も同様に300mgで再開する)。
出血時の対応
必要に応じて第VIIIまたは第IX因子製剤を併用可能。 出血部位や程度に応じ、 電子添文や最新ガイドラインに基づき最低用量を目安に投与する。
手術時の対応
大手術時は本剤を中止し、 凝固因子製剤による標準治療を行う。 再開時は血栓リスクや併用薬など全身状態を考慮する。 抜歯などの小手術では中止や用量変更は不要。
出典
1) ファイザー株式会社. ヒムペブジ®皮下注150mgペン 電子添文 2024年12月作成 (第1版)
最終更新日 : 2025年12月9日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Marstacimab
Marstacimab:マルスタシマブ(ヒムペブジ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 300mg 皮下注射 | ー | Day 1 |
| 150mg 皮下注射 | ー | Day 8、15… |
前投薬
その他
| 体重50kg以上で効果不十分な場合は、週1回300mgへの増量投与が可能 |
概要
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
抗TFPIモノクローナル抗体 マルスタシマブ
*ファイザー株式会社の外部サイトへ遷移します
投与スケジュール
血液凝固第Ⅷ因子又は第Ⅸ因子に対するインヒビターを保有しない先天性血友病患者における出血傾向の抑制

通常、 12歳以上かつ体重35kg以上の患者には、 Marstacimab (遺伝子組換え) として初回に300mgを皮下投与し、 以降は1週間隔で1回150mgを皮下投与する。 なお、 体重50kg以上で効果不十分な場合には、 1週間隔で1回300mgに増量して皮下投与できる。
ヒムペブジ皮下注150mgペン 添付文書¹⁾より引用
Key Data|臨床試験結果
📊 B7841005試験
ヒムペブジ皮下注150mgペン 添付文書¹⁾よりデータ引用
インヒビター非保有の中等症~重症血友病AまたはB患者を対象に、 Marstacimab皮下投与の有効性を、 出血時補充療法または定期補充療法を行っていた観察期間 (6ヵ月) とMarstacimab投与期間 (12ヵ月) の年換算出血率 (ABR) を比較して評価した。
【有効性】
年換算出血率 (ABR) 最小二乗平均値
● 導入前に出血時補充療法を受けた群 (33例)
- 導入前 [観察期間] : 39.86 回/年
- 導入後 [投与期間] : 3.20 回/年
● 導入前に定期補充療法を受けた群 (83例)
- 導入前 [観察期間] : 7.90 回/年
- 導入後 [投与期間] : 5.09 回/年
【安全性】
- 注射部位そう痒感 3.4%
- そう痒症 3.4%
- プロトロンビンフラグメント1・2増加 2.6%
- 注射部位紅斑 2.6%
特徴と注意点
🧑⚕️ヒムペブジ®は、 外因系血液凝固反応の主要な制御因子であるTFPIを阻害し、 外因系経路を増強することで、 血友病AおよびBの両方に有効な新規作用機序の薬剤です。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序

編集部作図
Marstacimabは、 組織因子経路インヒビター (TFPI) のKunitzドメイン2 (K2) を標的とするヒトモノクローナルIgG1抗体である。 TFPIはK2を介して活性型血液凝固第X因子に結合しこれを阻害するが、 MarstacimabはTFPIによるこの活性型第X因子の阻害を抑制することで、 外因系凝固経路を増強する。
適用時の注意事項
- 出血傾向の抑制を目的とした定期投与専用であり、 出血時の止血には使用しない
- 血液凝固第VIII因子または第IX因子製剤から切り替える際は、 前治療薬の半減期を考慮し、 適切な時期に中止する
- 非血液凝固因子製剤から切り替える際は、 前治療薬の半減期に基づき、 少なくとも半減期の5倍以上の休薬期間を設け、 必要に応じて凝固因子製剤による補充療法を行う
使用が想定される各血液凝固因子製剤および非血液凝固因子製剤の半減期については、 『ヒムペブジ®皮下注150mgペン 投与中の注意事項』の6~7ページに記載されている。
- 自己注射は、 十分な教育と訓練を実施し、 患者または介護者が確実に投与できることを確認したうえで、 医師の管理・指導のもとで実施する
- 本剤は冷蔵庫から出して直射日光を避けながら外箱のまま15~30分かけて自然に室温 (30℃以下) に戻す。 電子レンジや熱湯で温めないこと。 室温に戻した薬剤は再冷蔵せず、 7日以内に使用する。 振とうは避ける
- 注射部位は腹部または大腿前面から選択する。 腹部に投与する場合は、 座位で前かがみになり腹部をゆるめた姿勢で、 臍部から5cm以上離れた部位を選ぶ。 大腿前面に投与する場合も座位で行い、 毎回注射部位を変更することが望ましい。 300mgを投与する場合は、 150mgずつを2カ所の異なる部位に分けて投与する。
投与を忘れた場合の対応
投与予定日に投与できなかった場合は、 可能な限り速やかに予定用量で再開し、 以降は原則としてその日を起点に週1回の投与を継続する。
再開日が最終投与日から14日以上経過している場合は、 再開時の初回投与量を300mgとする (300mgで治療中の患者が14日以上投与を空けた場合も同様に300mgで再開する)。
出血時の対応
必要に応じて第VIIIまたは第IX因子製剤を併用可能。 出血部位や程度に応じ、 電子添文や最新ガイドラインに基づき最低用量を目安に投与する。
手術時の対応
大手術時は本剤を中止し、 凝固因子製剤による標準治療を行う。 再開時は血栓リスクや併用薬など全身状態を考慮する。 抜歯などの小手術では中止や用量変更は不要。
出典
1) ファイザー株式会社. ヒムペブジ®皮下注150mgペン 電子添文 2024年12月作成 (第1版)
最終更新日 : 2025年12月9日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。





