FOLFOX + Cmab
フルオロウラシル + レボホリナート + オキサリプラチン + セツキシマブ
Cmab:Cetuximab(アービタックス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| (1週間隔) 400mg/m² 点滴 | 1 | Day1 |
| (1週間隔) 250mg/m² 点滴 | 1 | Day8 |
| (1週間隔) 250mg/m² 点滴 | 2~ | Day 1,8 |
| (2週間隔) 500mg/m² 点滴 | 1~ | Day1 |
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 85mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 急速静注 | 1~ | Day1 |
| 2,400mg/m² 持続静注 | 1~ | Day1~3 |
前投薬
その他
| 1コース14日間。 |
| L-OHP+I−LVプラス5−FUをFOLFOX療法と呼ぶ。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*メルクバイオファーマ株式会社の外部サイトへ遷移します
用法用量
JACCROCC-05試験⁶⁾、 セツキシマブ電子添文⁴⁾の用法および用量
Cmab 1週間間隔
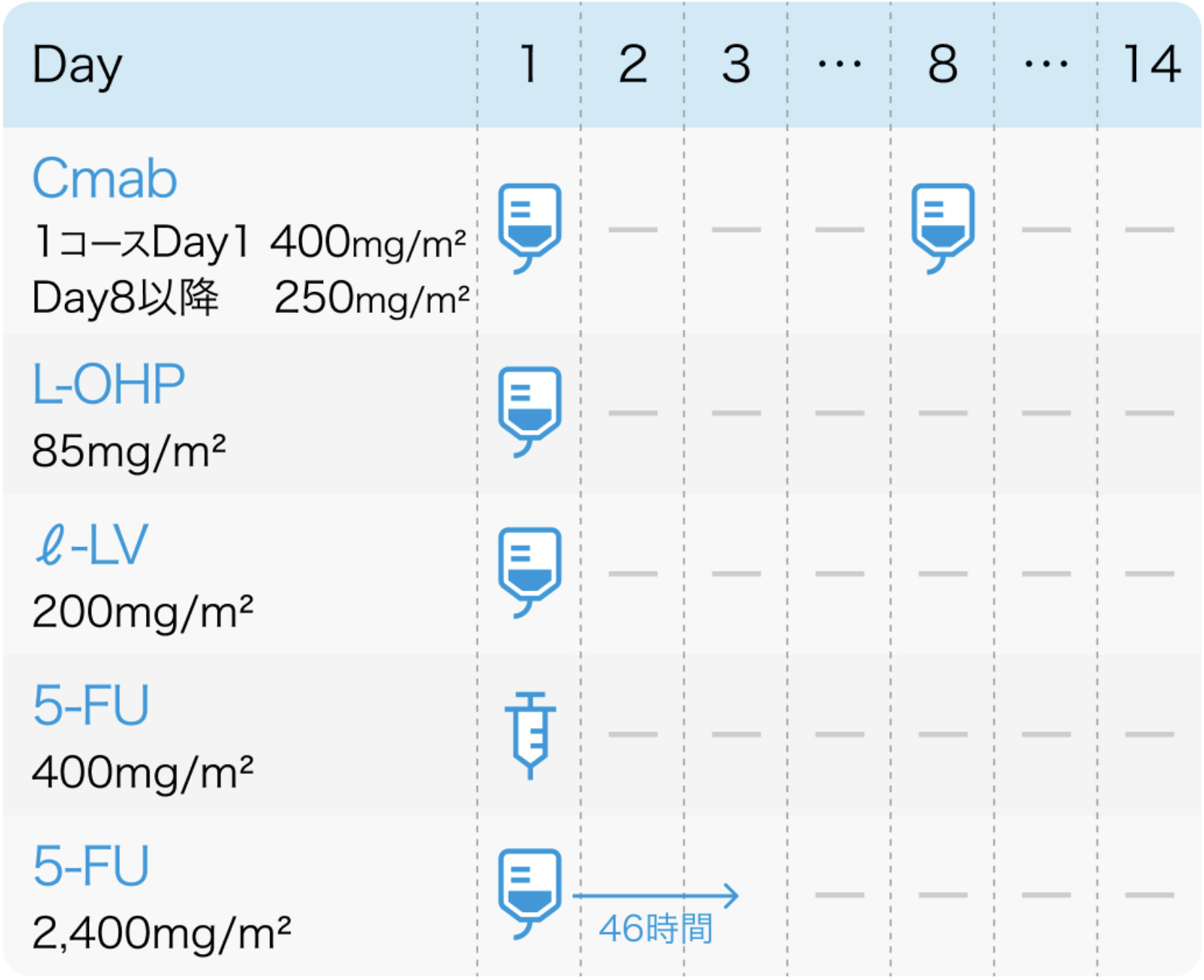
Target Oncol. 2016 Dec;11(6):799-806⁶⁾、 アービタックス®電子添文 (2023年12月改訂 第4版)⁴⁾より作図
Cmab 2週間間隔
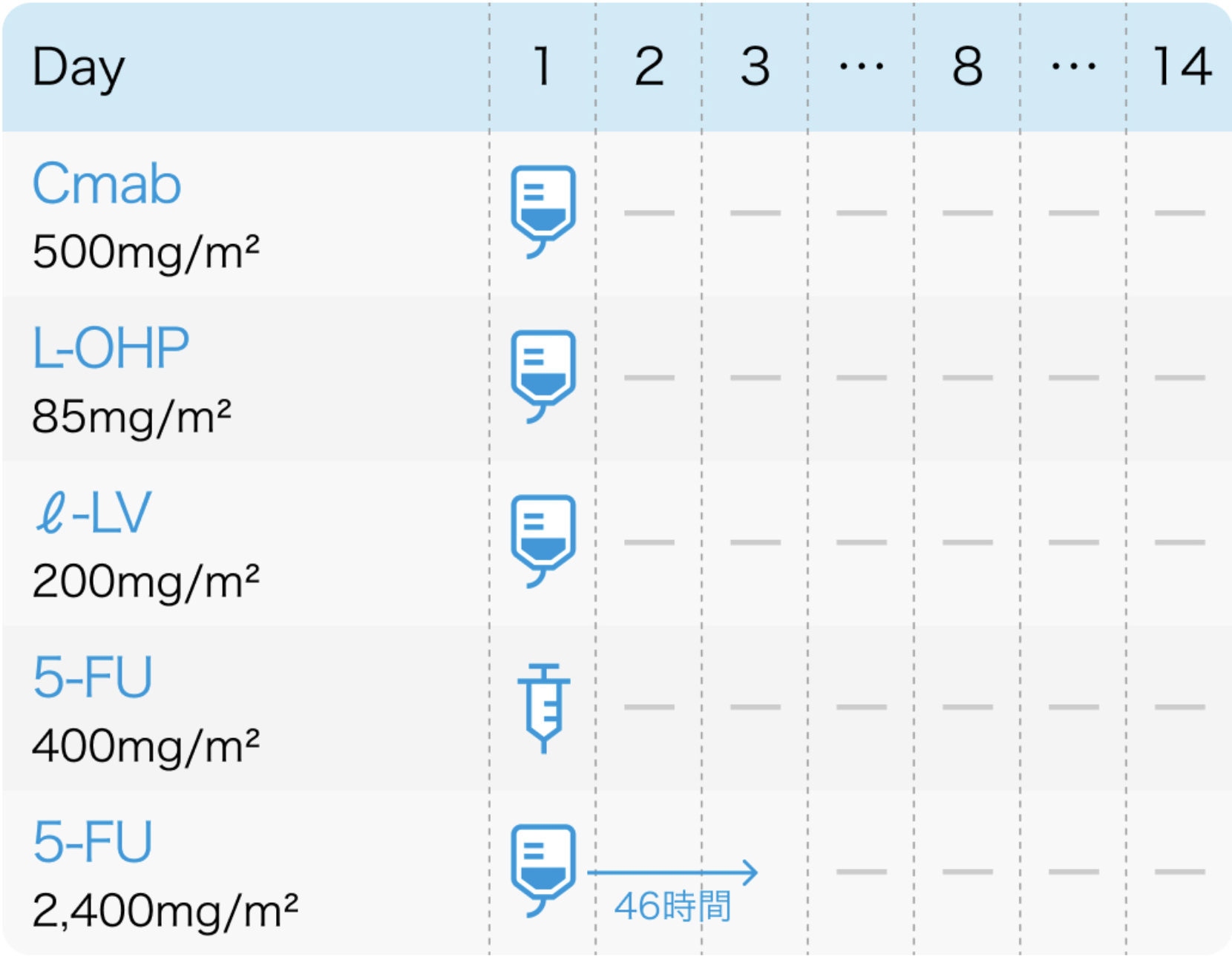
Target Oncol. 2016 Dec;11(6):799-806⁶⁾、 アービタックス®電子添文 (2023年12月改訂 第4版)⁴⁾より作図
投与開始基準
JACCROCC-05試験⁶⁾のプロトコル
免疫組織化学でEGFR発現を示す結腸または直腸の腺癌、 切除不能な転移を有するKRASエクソン2野生型腫瘍、 少なくとも1つの10mm以上の測定可能病変または残存する非測定可能病変がある20~79歳の患者
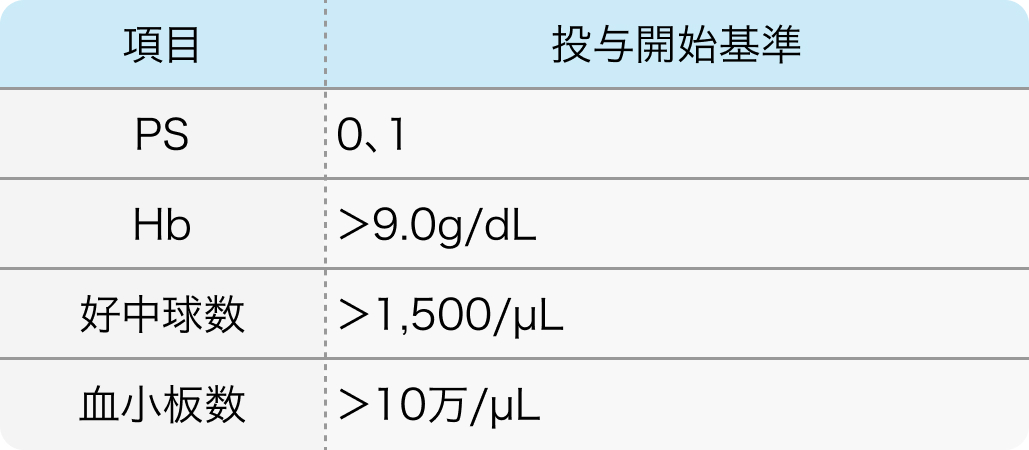
Target Oncol. 2016 Dec;11(6):799-806⁶⁾より作図
主な有害事象
JACCROCC-05試験⁶⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少症 76% (50%)
- 白血球球減少症 78% (22%)
- 血小板数減少 67% (7%)
- 下痢 46% (7%)
- AST上昇 67% (6%)
- ALT上昇 65% (6%)
- 倦怠感 46% (6%)
- 口腔粘膜炎 63% (6%)
- 貧血 48% (4%)
- 発熱性好中球減少症 4% (4%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢感覚神経障害 67% (20%)
- 手掌足底赤血球感覚異常 35% (7%)
Target Oncol. 2016 Dec;11(6):799-806⁶⁾より引用
上手に使うためのワンポイント
治療選択肢について
左側RAS/BRAF野生型・MSS・HER2陰性における第一選択肢。 右側で腫瘍縮小が必要と考えられる対象においても治療選択肢となりうる。
ETS、 DoRを求める場合の対応
Early Tumor Shrinkage (ETS) やDepth of Response (DoR) を求める時は、 隔週投与より毎週投与を推奨する医師もいる。 8週での腫瘍縮小が得られたあとは隔週投与に切り替えるなど、 長期投与を考慮した投与変更は選択肢となる。
悪心リスクが高い患者への対応
若年・女性などには、 初回投与時から選択的NK1受容体拮抗型制吐剤を前投薬として用いることを検討する。
高齢者への対応
JCOG1018試験⁸⁾では、 75歳以上もしくは、 70-74歳かつPS2の高齢患者では、 1次治療PFSにおけるオキサリプラチンの上乗せ効果は乏しいことが報告されている。 患者の身体及び腫瘍状況を考慮して治療方針を決定する必要がある。 FL+Pmabも治療選択肢となりうる。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
抗がん剤による末梢神経障害 (CIPN)
実臨床では、 末梢神経障害 (CIPN) の評価に、 CTCAEよりも症状の期間と程度を加味したDebiopharm社神経症状-感覚性毒性基準 (DEB-NTC) を用いる。 コンバージョンが明らかに困難と思われ、 延命を目的とするような症例では、 QOL低下を考慮して、 OPTIMOX1³⁾に準じたオキサリプラチン計画中止も積極的に検討する。
*CIPN : chemotherapy-induced peripheral neuropathies **DEB-NTC : Debiopharm Neurotoxicity Criteria of Debiopharm

減量・休薬・中止のポイント
好中球数の投与開始基準は 一般的に1500/μL以上だが、 複数回数投与によりその患者の毒性プロファイルがある程度予想できる場合には、 好中球数1200/μL前後でも投与可能とする医師はいる。
早期腫瘍縮小が得られ、 かつ抗EGFR抗体による毒性が患者にとって強いと感じられる時には抗EGFR抗体の一時休薬や終了も選択肢となりうる。
皮膚障害の対策
抗EGFR抗体による皮膚障害に対してJ-STEPP試験に準じた予防策も考慮する。 特にJ-STEPP試験に準じた予防策を行わないときは、 治療開始早期は抗EGFR抗体による皮膚障害のケアに注力する。
J-STEPP試験 : Panitumumabを含む治療投与前日から8週間、 保湿剤と日焼け止め (SPF25、 PFA4~8)、 0.5%ヒドロコルチゾンクリ‐ムを1日2回局所に塗布、 ミノサイクリン100㎎/日を1日1回内服
低Mg血症の出現に注意
治療期間が長くなる1次治療では抗EGFR抗体による低Mg血症の出現に注意する。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験①|JACCROCC-05試験⁶⁾
KRAS exon 2野生型で未治療の転移性大腸癌患者に対するFOLFOX (フルオロウラシル、 レボホリナート、 オキサリプラチン)+セツキシマブ (Cmab) 併用療法の第II相試験の結果から、 早期腫瘍縮小を得た患者では無増悪生存期間 (PFS) と全生存期間 (OS) の有意な延長を認めた。 腫瘍縮小を得ることの臨床的重要性は、 治療前の腫瘍径によって異なる可能性が示された。
ORR
66.7%
(95%CI 53.4-77.8%)
病勢コントロール率
85.2%
(95%CI 73.4-92.3%)
PFS中央値
11.1ヵ月
(95%CI 8.0ー13.5ヵ月)
ETS vs 非ETS
ETS : 11.3ヵ月
非ETS : 3.7ヵ月
HR 0.26 (95%CI 0.13-0.61)、 p=0.0003
OS中央値
33.9ヵ月
(95%CI 26.5-43.6ヵ月)
ETS vs 非ETS
ETS : 42.8ヵ月
非ETS : 9.0ヵ月
HR 0.40 (95%CI 0.18-0.99)、 p=0.0279
ETS率
80%
評価可能であった50例が対象
腫瘍縮小率中央値
56.3%
(範囲 -31%-100%)
関連する臨床試験②|TAILOR試験⁷⁾
RAS遺伝子野生型で未治療の転移性大腸癌患者において、 FOLFOX4(フルオロウラシル+レボホリナート+オキサリプラチン)+セツキシマブ (Cmab) の効果を、 FOLFOX4単独を対照に検証した第Ⅲ相試験TAILORの結果より、 FOLFOX4に比べて無増悪生存期間 (PFS) ならびに全生存期間 (OS) の有意な改善が示された。
PFS中央値
- FOLFOX4+Cmab群 : 9.2ヵ月
(95%CI 7.7-9.4ヵ月)
- FOLFOX4群 : 7.4ヵ月
(95%CI 5.6-7.9ヵ月)
HR 0.69 (95%CI 0.54-0.89)、 p=0.004
PFSのサブ解析
BRAF変異例ではFOLFOX4群の方が良好な成績だった
(n = 52)
HR 2.01 (95%CI 1.08-3.73)
OS中央値
- FOLFOX4+Cmab群 : 20.7ヵ月
(95%CI 15.9-22.1ヵ月)
- FOLFOX4群 : 17.8ヵ月
(95%CI 14.9-19.6ヵ月)
HR 0.76 (95%CI 0.61-0.96)、 p=0.02
ORR
- FOLFOX4+Cmab群 : 61.1%
- FOLFOX4群 : 39.5%
OR 2.41 (95%CI 1.61-3.61)、 p<0.001
出典
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/5/10]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/15]
- 協和キリン株式会社. 5-FU®電子添文 (2024年3月改訂 第3版) [最終閲覧 : 2024/04/01]
- メルクバイオファーマ株式会社. アービタックス®電子添文 (2023年12月改訂 第4版) [最終閲覧 : 2024/7/12]
- メルクバイオファーマ株式会社. アービタックス®適正使用ガイド (2023年12月作成) [最終閲覧 : 2024/7/12]
- Early Tumor Shrinkage and Depth of Response as Predictors of Favorable Treatment Outcomes in Patients with Metastatic Colorectal Cancer Treated with FOLFOX Plus Cetuximab (JACCRO CC-05). Target Oncol. 2016 Dec;11(6):799-806. PMID: 27306648
- Efficacy and Tolerability of First-Line Cetuximab Plus Leucovorin, Fluorouracil, and Oxaliplatin (FOLFOX-4) Versus FOLFOX-4 in Patients With RAS Wild-Type Metastatic Colorectal Cancer: The Open-Label, Randomized, Phase III TAILOR Trial. J Clin Oncol. 2018 Oct 20;36(30):3031-3039. PMID: 30199311
- JCOG1018 : 「高齢切除不能進行大腸癌に対する全身化学療法に関するランダム化比較第 III 相試験」 . 総括報告書 (作成日 : 2022年1月4日)
最終更新日 : 2024年8月21日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
FOLFOX + Cmab
Cmab:Cetuximab(アービタックス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| (1週間隔) 400mg/m² 点滴 | 1 | Day1 |
| (1週間隔) 250mg/m² 点滴 | 1 | Day8 |
| (1週間隔) 250mg/m² 点滴 | 2~ | Day 1,8 |
| (2週間隔) 500mg/m² 点滴 | 1~ | Day1 |
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 85mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 急速静注 | 1~ | Day1 |
| 2,400mg/m² 持続静注 | 1~ | Day1~3 |
前投薬
その他
| 1コース14日間。 |
| L-OHP+I−LVプラス5−FUをFOLFOX療法と呼ぶ。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*メルクバイオファーマ株式会社の外部サイトへ遷移します
用法用量
JACCROCC-05試験⁶⁾、 セツキシマブ電子添文⁴⁾の用法および用量
Cmab 1週間間隔

Target Oncol. 2016 Dec;11(6):799-806⁶⁾、 アービタックス®電子添文 (2023年12月改訂 第4版)⁴⁾より作図
Cmab 2週間間隔

Target Oncol. 2016 Dec;11(6):799-806⁶⁾、 アービタックス®電子添文 (2023年12月改訂 第4版)⁴⁾より作図
投与開始基準
JACCROCC-05試験⁶⁾のプロトコル
免疫組織化学でEGFR発現を示す結腸または直腸の腺癌、 切除不能な転移を有するKRASエクソン2野生型腫瘍、 少なくとも1つの10mm以上の測定可能病変または残存する非測定可能病変がある20~79歳の患者

Target Oncol. 2016 Dec;11(6):799-806⁶⁾より作図
主な有害事象
JACCROCC-05試験⁶⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少症 76% (50%)
- 白血球球減少症 78% (22%)
- 血小板数減少 67% (7%)
- 下痢 46% (7%)
- AST上昇 67% (6%)
- ALT上昇 65% (6%)
- 倦怠感 46% (6%)
- 口腔粘膜炎 63% (6%)
- 貧血 48% (4%)
- 発熱性好中球減少症 4% (4%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢感覚神経障害 67% (20%)
- 手掌足底赤血球感覚異常 35% (7%)
Target Oncol. 2016 Dec;11(6):799-806⁶⁾より引用
上手に使うためのワンポイント
治療選択肢について
左側RAS/BRAF野生型・MSS・HER2陰性における第一選択肢。 右側で腫瘍縮小が必要と考えられる対象においても治療選択肢となりうる。
ETS、 DoRを求める場合の対応
Early Tumor Shrinkage (ETS) やDepth of Response (DoR) を求める時は、 隔週投与より毎週投与を推奨する医師もいる。 8週での腫瘍縮小が得られたあとは隔週投与に切り替えるなど、 長期投与を考慮した投与変更は選択肢となる。
悪心リスクが高い患者への対応
若年・女性などには、 初回投与時から選択的NK1受容体拮抗型制吐剤を前投薬として用いることを検討する。
高齢者への対応
JCOG1018試験⁸⁾では、 75歳以上もしくは、 70-74歳かつPS2の高齢患者では、 1次治療PFSにおけるオキサリプラチンの上乗せ効果は乏しいことが報告されている。 患者の身体及び腫瘍状況を考慮して治療方針を決定する必要がある。 FL+Pmabも治療選択肢となりうる。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
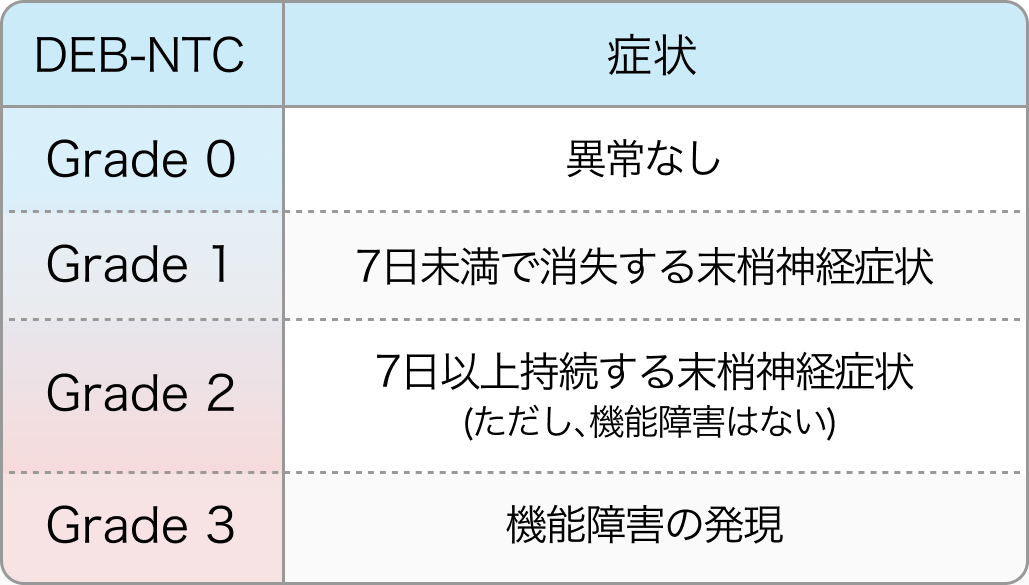
抗がん剤による末梢神経障害 (CIPN)
実臨床では、 末梢神経障害 (CIPN) の評価に、 CTCAEよりも症状の期間と程度を加味したDebiopharm社神経症状-感覚性毒性基準 (DEB-NTC) を用いる。 コンバージョンが明らかに困難と思われ、 延命を目的とするような症例では、 QOL低下を考慮して、 OPTIMOX1³⁾に準じたオキサリプラチン計画中止も積極的に検討する。
*CIPN : chemotherapy-induced peripheral neuropathies **DEB-NTC : Debiopharm Neurotoxicity Criteria of Debiopharm


減量・休薬・中止のポイント
好中球数の投与開始基準は 一般的に1500/μL以上だが、 複数回数投与によりその患者の毒性プロファイルがある程度予想できる場合には、 好中球数1200/μL前後でも投与可能とする医師はいる。
早期腫瘍縮小が得られ、 かつ抗EGFR抗体による毒性が患者にとって強いと感じられる時には抗EGFR抗体の一時休薬や終了も選択肢となりうる。
皮膚障害の対策
抗EGFR抗体による皮膚障害に対してJ-STEPP試験に準じた予防策も考慮する。 特にJ-STEPP試験に準じた予防策を行わないときは、 治療開始早期は抗EGFR抗体による皮膚障害のケアに注力する。
J-STEPP試験 : Panitumumabを含む治療投与前日から8週間、 保湿剤と日焼け止め (SPF25、 PFA4~8)、 0.5%ヒドロコルチゾンクリ‐ムを1日2回局所に塗布、 ミノサイクリン100㎎/日を1日1回内服
低Mg血症の出現に注意
治療期間が長くなる1次治療では抗EGFR抗体による低Mg血症の出現に注意する。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験①|JACCROCC-05試験⁶⁾
KRAS exon 2野生型で未治療の転移性大腸癌患者に対するFOLFOX (フルオロウラシル、 レボホリナート、 オキサリプラチン)+セツキシマブ (Cmab) 併用療法の第II相試験の結果から、 早期腫瘍縮小を得た患者では無増悪生存期間 (PFS) と全生存期間 (OS) の有意な延長を認めた。 腫瘍縮小を得ることの臨床的重要性は、 治療前の腫瘍径によって異なる可能性が示された。
ORR
66.7%
(95%CI 53.4-77.8%)
病勢コントロール率
85.2%
(95%CI 73.4-92.3%)
PFS中央値
11.1ヵ月
(95%CI 8.0ー13.5ヵ月)
ETS vs 非ETS
ETS : 11.3ヵ月
非ETS : 3.7ヵ月
HR 0.26 (95%CI 0.13-0.61)、 p=0.0003
OS中央値
33.9ヵ月
(95%CI 26.5-43.6ヵ月)
ETS vs 非ETS
ETS : 42.8ヵ月
非ETS : 9.0ヵ月
HR 0.40 (95%CI 0.18-0.99)、 p=0.0279
ETS率
80%
評価可能であった50例が対象
腫瘍縮小率中央値
56.3%
(範囲 -31%-100%)
関連する臨床試験②|TAILOR試験⁷⁾
RAS遺伝子野生型で未治療の転移性大腸癌患者において、 FOLFOX4(フルオロウラシル+レボホリナート+オキサリプラチン)+セツキシマブ (Cmab) の効果を、 FOLFOX4単独を対照に検証した第Ⅲ相試験TAILORの結果より、 FOLFOX4に比べて無増悪生存期間 (PFS) ならびに全生存期間 (OS) の有意な改善が示された。
PFS中央値
- FOLFOX4+Cmab群 : 9.2ヵ月
(95%CI 7.7-9.4ヵ月)
- FOLFOX4群 : 7.4ヵ月
(95%CI 5.6-7.9ヵ月)
HR 0.69 (95%CI 0.54-0.89)、 p=0.004
PFSのサブ解析
BRAF変異例ではFOLFOX4群の方が良好な成績だった
(n = 52)
HR 2.01 (95%CI 1.08-3.73)
OS中央値
- FOLFOX4+Cmab群 : 20.7ヵ月
(95%CI 15.9-22.1ヵ月)
- FOLFOX4群 : 17.8ヵ月
(95%CI 14.9-19.6ヵ月)
HR 0.76 (95%CI 0.61-0.96)、 p=0.02
ORR
- FOLFOX4+Cmab群 : 61.1%
- FOLFOX4群 : 39.5%
OR 2.41 (95%CI 1.61-3.61)、 p<0.001
出典
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/5/10]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/15]
- 協和キリン株式会社. 5-FU®電子添文 (2024年3月改訂 第3版) [最終閲覧 : 2024/04/01]
- メルクバイオファーマ株式会社. アービタックス®電子添文 (2023年12月改訂 第4版) [最終閲覧 : 2024/7/12]
- メルクバイオファーマ株式会社. アービタックス®適正使用ガイド (2023年12月作成) [最終閲覧 : 2024/7/12]
- Early Tumor Shrinkage and Depth of Response as Predictors of Favorable Treatment Outcomes in Patients with Metastatic Colorectal Cancer Treated with FOLFOX Plus Cetuximab (JACCRO CC-05). Target Oncol. 2016 Dec;11(6):799-806. PMID: 27306648
- Efficacy and Tolerability of First-Line Cetuximab Plus Leucovorin, Fluorouracil, and Oxaliplatin (FOLFOX-4) Versus FOLFOX-4 in Patients With RAS Wild-Type Metastatic Colorectal Cancer: The Open-Label, Randomized, Phase III TAILOR Trial. J Clin Oncol. 2018 Oct 20;36(30):3031-3039. PMID: 30199311
- JCOG1018 : 「高齢切除不能進行大腸癌に対する全身化学療法に関するランダム化比較第 III 相試験」 . 総括報告書 (作成日 : 2022年1月4日)
最終更新日 : 2024年8月21日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。






