CAPOX + T-mab
カペシタビン + オキサリプラチン + トラスツズマブ
治療スケジュール
概要
監修医師
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 130mg/m² 点滴 | 1~ | Day1 |
Tmab:Trastuzumab(ハーセプチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 8mg/kg 点滴 | 1 | Day1 |
| 6mg/kg 点滴 | 2~ | Day1 |
Cape:Capecitabine(ゼローダ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2,000mg/m² 経口分2 朝夕食後 | 1~ | Day1~14 |
前投薬
その他
| 1コース21日間。 |
| L-OHP+ CapeをCAPOXと呼ぶ。 |
CAPOX + T-mabの全コンテンツはアプリからご利用いただけます。
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*チェプラファームの外部サイトへ遷移します
*中外製薬株式会社の外部サイトへ遷移します
用法用量
多施設共同第II相試験⁶⁾のプロトコル

Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より作図
投与開始基準
トラスツズマブ適正使用ガイド⁵⁾の基準
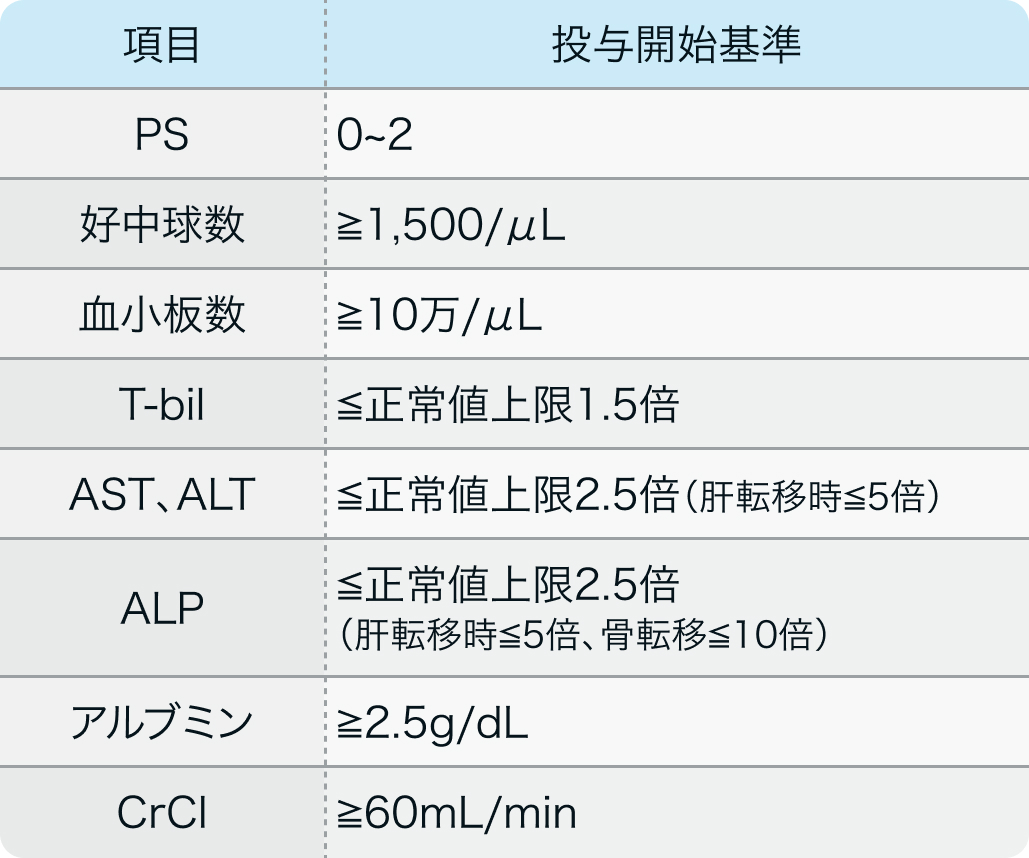
ハーセプチン®安全性情報 (2023年3月改訂) より作図
中止基準
多施設共同第II相試験⁶⁾のプロトコル
- Grade3~4の血液学的毒性 (貧血を除く)
- Grade2~4の非血液学的毒性
- CAPOX療法が3週間以上中断された場合、 CAPOX療法は永久に中止
毒性が化学療法に起因する場合、 トラスツズマブの投与は継続を考慮
Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より引用
主な有害事象
多施設共同第II相試験⁶⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少 56.4% (18.2%)
- 貧血 96.4% (10.9%)
- 血小板減少症 67.3% (3.6%)
- 白血球減少症 49.1% (0%)
- 悪心 54.5% (1.8%)
- 嘔吐 32.7% (0%)
- 下痢 38.2% (1.8%)
- 便秘 30.9% (0%)
- 口内炎 21.8% (1.8%)
- 倦怠感 54.5% (5.5%)
- 体重減少 14.5% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢性ニューロパチー 70.9% (10.9%)
- 手足症候群 32.7% (1.8%)
Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より引用
上手に使うためのワンポイント
- 胃癌は治療開始時にすでに体重減少を伴っていることが多いこと、 狭窄・腹膜播種など催吐リスクが高いことから、 オキサリプラチン130mg/m²で投与する場合には特に、 CINV予防として3剤併用 (NK1拮抗薬+5HT3拮抗薬+ステロイド) を考慮する。
- オキサリプラチンによるCIPNにより、 2次治療のPTX投与が困難になる時がある。 治療効果が十分と考えられ、 CIPN Grade2となった場合は、 オキサリプラチンの中止を考慮する。 上記を考慮しオキサリプラチンについては計画中止も治療選択肢と考えられる。
- カペシタビンによる手足症候群の症状と、 オキサリプラチンによるCIPNの症状がオーバーラップするため問診時には混同しないように注意する。
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
- ガイドラインでは、 HER2陽性胃癌1次治療において 「推奨される化学療法レジメン」 である。 通常の術後再発例はもちろん、 術後補助療法S-1に不応となった早期再発例に対するXParTS試験の結果から、 早期再発例の第一選択とする医師もいる。 国内での臨床試験結果がないため、 韓国での第Ⅱ相試験⁶⁾の結果がリファレンスとなる。
- オキサリプラチンの併用が必要なためvulnerableな高齢患者への適用には注意が必要である。 CAPOXは国内でも大腸癌の場合、 オキサリプラチンの初回投与量は130mg/m²だが、 70歳以上高齢者を対象としたTCOG GI-1601試験⁷⁾の初期解析において毒性により両薬剤の1段階減量による継続を結論づけられた。 S-1におけるWJOG8315G⁸⁾の結果と合わせて、 高齢者の初回投与量は100mg/m²が妥当かもしれない。
- トラスツズマブは心毒性を有する。 治療開始前に心エコーを実施し、 LVEF<50%の症例には投与しない。 おおよそ3ヵ月程度の間隔で、 心エコーで心機能のスクリーニングを行う。
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験
多施設共同第II相試験⁶⁾
進行胃がんに対するトラスツズマブとカペシタビンおよびオキサリプラチンの併用療法の多施設共同第II相試験。 主要評価項目は奏効率 (ORR) で、 副次評価項目には無増悪生存期間 (PFS)、 全生存期間 (OS)、 毒性プロファイルが含まれた。
Eur J Cancer. 2015 Mar;51(4):482-488.
出典
- チェプラファーム. ゼローダ®電子添文 (2024年2月改訂 第3版) [最終閲覧 : 2024/5/10]
- チェプラファーム. ゼローダ®適正使用ガイド (2024年2月改訂) [最終閲覧 : 2024/5/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/17]
- 中外製薬株式会社. ハーセプチン®電子添文 (2022年12月改訂 第5版) [最終閲覧 : 2024/6/18]
- 中外製薬株式会社. ハーセプチン®安全性情報 (2023年12月改訂) [最終閲覧 : 2024/6/18]
- Multicenter phase II study of trastuzumab in combination with capecitabine and oxaliplatin for advanced gastric cancer. Eur J Cancer. 2015 Mar;51(4):482-488. PMID: 25661103
- Multicenter phase II study of capecitabine plus oxaliplatin in older patients with advanced gastric cancer: the Tokyo Cooperative Oncology Group (TCOG) GI-1601 study. Gastric Cancer. 2023 Nov;26(6):1020-1029. PMID: 37610558
- A randomized phase II study comparing S-1 plus oxaliplatin with S-1 monotherapy for elderly patients with advanced gastric cancer: WJOG8315G. JSMO 2023.
最終更新日 : 2024年7月1日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
CAPOX + T-mabの全コンテンツはアプリからご利用いただけます。
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
CAPOX + T-mab
カペシタビン + オキサリプラチン + トラスツズマブ
2024年07月02日更新
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 130mg/m² 点滴 | 1~ | Day1 |
Tmab:Trastuzumab(ハーセプチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 8mg/kg 点滴 | 1 | Day1 |
| 6mg/kg 点滴 | 2~ | Day1 |
Cape:Capecitabine(ゼローダ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2,000mg/m² 経口分2 朝夕食後 | 1~ | Day1~14 |
前投薬
その他
| 1コース21日間。 |
| L-OHP+ CapeをCAPOXと呼ぶ。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*チェプラファームの外部サイトへ遷移します
*中外製薬株式会社の外部サイトへ遷移します
用法用量
多施設共同第II相試験⁶⁾のプロトコル

Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より作図
投与開始基準
トラスツズマブ適正使用ガイド⁵⁾の基準

ハーセプチン®安全性情報 (2023年3月改訂) より作図
中止基準
多施設共同第II相試験⁶⁾のプロトコル
- Grade3~4の血液学的毒性 (貧血を除く)
- Grade2~4の非血液学的毒性
- CAPOX療法が3週間以上中断された場合、 CAPOX療法は永久に中止
毒性が化学療法に起因する場合、 トラスツズマブの投与は継続を考慮
Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より引用
主な有害事象
多施設共同第II相試験⁶⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少 56.4% (18.2%)
- 貧血 96.4% (10.9%)
- 血小板減少症 67.3% (3.6%)
- 白血球減少症 49.1% (0%)
- 悪心 54.5% (1.8%)
- 嘔吐 32.7% (0%)
- 下痢 38.2% (1.8%)
- 便秘 30.9% (0%)
- 口内炎 21.8% (1.8%)
- 倦怠感 54.5% (5.5%)
- 体重減少 14.5% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢性ニューロパチー 70.9% (10.9%)
- 手足症候群 32.7% (1.8%)
Eur J Cancer. 2015 Mar;51(4):482-488⁶⁾より引用
上手に使うためのワンポイント
- 胃癌は治療開始時にすでに体重減少を伴っていることが多いこと、 狭窄・腹膜播種など催吐リスクが高いことから、 オキサリプラチン130mg/m²で投与する場合には特に、 CINV予防として3剤併用 (NK1拮抗薬+5HT3拮抗薬+ステロイド) を考慮する。
- オキサリプラチンによるCIPNにより、 2次治療のPTX投与が困難になる時がある。 治療効果が十分と考えられ、 CIPN Grade2となった場合は、 オキサリプラチンの中止を考慮する。 上記を考慮しオキサリプラチンについては計画中止も治療選択肢と考えられる。
- カペシタビンによる手足症候群の症状と、 オキサリプラチンによるCIPNの症状がオーバーラップするため問診時には混同しないように注意する。
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
- ガイドラインでは、 HER2陽性胃癌1次治療において 「推奨される化学療法レジメン」 である。 通常の術後再発例はもちろん、 術後補助療法S-1に不応となった早期再発例に対するXParTS試験の結果から、 早期再発例の第一選択とする医師もいる。 国内での臨床試験結果がないため、 韓国での第Ⅱ相試験⁶⁾の結果がリファレンスとなる。
- オキサリプラチンの併用が必要なためvulnerableな高齢患者への適用には注意が必要である。 CAPOXは国内でも大腸癌の場合、 オキサリプラチンの初回投与量は130mg/m²だが、 70歳以上高齢者を対象としたTCOG GI-1601試験⁷⁾の初期解析において毒性により両薬剤の1段階減量による継続を結論づけられた。 S-1におけるWJOG8315G⁸⁾の結果と合わせて、 高齢者の初回投与量は100mg/m²が妥当かもしれない。
- トラスツズマブは心毒性を有する。 治療開始前に心エコーを実施し、 LVEF<50%の症例には投与しない。 おおよそ3ヵ月程度の間隔で、 心エコーで心機能のスクリーニングを行う。
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験
多施設共同第II相試験⁶⁾
進行胃がんに対するトラスツズマブとカペシタビンおよびオキサリプラチンの併用療法の多施設共同第II相試験。 主要評価項目は奏効率 (ORR) で、 副次評価項目には無増悪生存期間 (PFS)、 全生存期間 (OS)、 毒性プロファイルが含まれた。
Eur J Cancer. 2015 Mar;51(4):482-488.
出典
- チェプラファーム. ゼローダ®電子添文 (2024年2月改訂 第3版) [最終閲覧 : 2024/5/10]
- チェプラファーム. ゼローダ®適正使用ガイド (2024年2月改訂) [最終閲覧 : 2024/5/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/17]
- 中外製薬株式会社. ハーセプチン®電子添文 (2022年12月改訂 第5版) [最終閲覧 : 2024/6/18]
- 中外製薬株式会社. ハーセプチン®安全性情報 (2023年12月改訂) [最終閲覧 : 2024/6/18]
- Multicenter phase II study of trastuzumab in combination with capecitabine and oxaliplatin for advanced gastric cancer. Eur J Cancer. 2015 Mar;51(4):482-488. PMID: 25661103
- Multicenter phase II study of capecitabine plus oxaliplatin in older patients with advanced gastric cancer: the Tokyo Cooperative Oncology Group (TCOG) GI-1601 study. Gastric Cancer. 2023 Nov;26(6):1020-1029. PMID: 37610558
- A randomized phase II study comparing S-1 plus oxaliplatin with S-1 monotherapy for elderly patients with advanced gastric cancer: WJOG8315G. JSMO 2023.
最終更新日 : 2024年7月1日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
CAPOX + T-mabの全コンテンツはアプリからご利用いただけます。
臨床支援アプリHOKUTOをダウンロードしてご覧ください。
今すぐ無料ダウンロード!
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。





