Durvalumab+CDDP(CBDCA)/Etop
デュルバルマブ+シスプラチン(カルボプラチン)/エトポシド
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
イミフィンジ®点滴静注 (デュルバルマブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】3週間 → 4週間 (維持療法)
【催吐性】 CDDP 高度、 CBDCA 中等度
【FN発症】中間リスク
CASPIAN試験³⁻⁵⁾ (1~4コース目)

CASPIAN試験³⁻⁵⁾ (5コース目~ 維持療法)

Lancet. 2019 Nov 23;394(10212):1929-1939. より引用
CBDCAはAUC6も承認されている。 4コース終了後のCT評価でSD以上であればDurvalumab単剤のみによる維持療法を4週ごとに行い、 PDまで繰り返す。 Durvalumabは体重30kg以下の場合の1回投与量は20mg/kg (体重) とする。 [電子添文記載]
KeyData|臨床試験結果
📊CASPIAN試験³⁻⁵⁾ >>詳しくみる
化学療法歴のないPS 0-1のED-SCLC患者805例を対象に、DurvalumabまたはDurvalumab+Tremelimumabとプラチナ製剤併用療法比較した国際共同第Ⅲ相試験
主要評価項目 : 全生存期間 (OS)³⁾
- Durvalumab併用群 : 13.0ヵ月
- プラチナ製剤併用療法群 : 10.3ヵ月
HR 0.73 [95%CI 0.591~0.909] p=0.0047
副次評価項目 : 無増悪生存期間 (PFS)³⁾
- Durvalumab併用群 : 5.1ヵ月
- プラチナ製剤併用療法群 : 5.4ヵ月
HR 0.73 [95%CI 0.65-0.94]
更新された報告 : 18ヵ月OS率⁴⁾
- Durvalumab併用群 : 32.0%
- プラチナ製剤併用療法群 : 24.8%
HR 0.75 [95%CI : 0.62-0.91]
更新された報告 : 36ヵ月OS率⁵⁾
- Durvalumab併用群 : 17.6%
- プラチナ製剤併用療法群 : 15.8%
HR 0.71 [95%CI : 0.60-0.86]
日本人集団のサブ解析⁶⁾
- OS : HR 0.77 ([95%CI 0.26‒2.26] 未達 vs 15.2ヵ月)
- PFS : HR 0.90 ([95%CI 0.43‒1.89])
- 毒性に関して全体集団と同様の傾向
各プロトコル
以下はCASPIAN試験³⁻⁵⁾より引用
投与開始基準例
- 好中球数≧1500/mm³
- 血小板数≧100,000/mm³
- ヘモグロビン≧9.0g/dL
- 血清ビリルビン≦1.5×正常域上限(ULN)
- AST / ALT / ALP ≦2.5×ULN
肝転移時は≦5×ULN
- クレアチニンクリアランス
- シスプラチン投与 >60mL/min
- カルボプラチン投与 >45mL/min
レジメンの特徴と注意点
肺癌診療ガイドライン2025の推奨³⁾
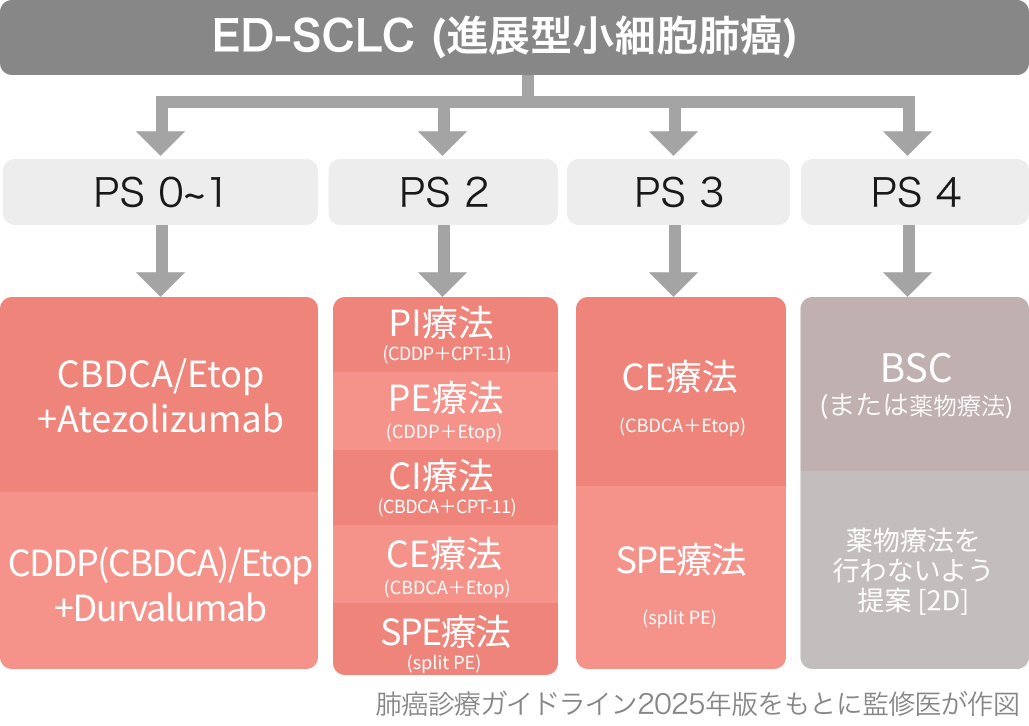
進展型小細胞肺癌 (PS 0-1) には、 プラチナ製剤/エトポシド併用療法+PD-L1阻害薬の併用治療を行うよう強く推奨 (1A)
投与開始前の注意点
- CBDCA、CDDPによるアレルギー歴を確認。
- PSが0~1が治験時の患者登録基準である。
- 自己免疫疾患、 間質性肺疾患等の既往がある患者はirAEのリスク因子となるため投与前に事前に評価を行う。
- 4コース終了後はPD、 有害事象あるいは臨床上の利益がない状況となるまでデュルバルマブ単剤での維持療法の継続について判断が必要なことに留意する。
副作用と対策
- 本剤のT細胞活性化作用により、 過度の免疫反応に起因すると考えられる様々な疾患や病態 (irAE) が現れることがある。
- CBDCAとアミノグリコシド系抗菌薬の併用によって聴覚障害や腎毒性が増強する可能性があるため注意。
- 内分泌機能検査 (TSH、 FT4、 ACTHなど) を定期的に実施し、モニタリングする。
- その他尿検査や画像評価などの定期的なモニタリングも必要である。
- 有害事象が疑われた場合には、 各専門医へのコンサルトも検討する。
使用上のワンポイント
ED-SCLCは根治不能であり、 患者のQOL改善と生存期問延長を重視した選択が重要。 PS良好例では、 第一選択として以下の理由から白金製剤併用+ICIが挙がる。 ICIが併用できないときや、間質性肺疾患合併時にはIP療法またはPE療法が候補となる。
IP療法 (CDDP+CPT-11) が標準であった
📊JCOG9511試験
PS0~2の70歳以下を対象として、 IP療法 (CDDP+CPT-11)とPE療法 (CDDP+ETP)と比較した第Ⅲ相試験。 2回目の中間解析で有効中止され、 IP療法が優越性を示した。 OS中央値 : 12.8ヵ月 vs 9.4ヵ月。
その後、白金製剤併用+ICIが標準療法に
📊IMpower133試験
CE療法 +Atezolizumabが、 CE療法に対してOSを優位に延長した。 OS中央値 : 12.3ヵ月 vs 10.3ヵ月。
📊CASPIAN試験
PE/CE療法+Durvalumabが、 PE/CE療法に対してOSを優位に延長した。 OS中央値 : 13.0ヵ月 vs 10.3ヵ月。
ICIそれぞれの併用療法比較
1.維持療法中の投与間隔が異なる
- CASPIAN試験 : Durvalumab 4週
- IMpower133試験 : Atezolizumab 3週
2.CASPIAN試験ではCDDPの使用が可能
直接比較した臨床試験はないが、 いずれの薬剤もPD-L1阻害薬であり、 効果・副作用に関しても同様と考えられる。
出典
1) アストラゼネカ株式会社 「イミフィンジ®︎、 イジュド®︎適正使用ガイド」 (2025年9月作成) [最終閲覧 2025/10/19]
*アストラゼネカ株式会社の外部サイトへ遷移します
2) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2025年10月19日
HOKUTO編集部医師監修
Durvalumab+CDDP(CBDCA)/Etop
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
イミフィンジ®点滴静注 (デュルバルマブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】3週間 → 4週間 (維持療法)
【催吐性】 CDDP 高度、 CBDCA 中等度
【FN発症】中間リスク
CASPIAN試験³⁻⁵⁾ (1~4コース目)

CASPIAN試験³⁻⁵⁾ (5コース目~ 維持療法)

Lancet. 2019 Nov 23;394(10212):1929-1939. より引用
CBDCAはAUC6も承認されている。 4コース終了後のCT評価でSD以上であればDurvalumab単剤のみによる維持療法を4週ごとに行い、 PDまで繰り返す。 Durvalumabは体重30kg以下の場合の1回投与量は20mg/kg (体重) とする。 [電子添文記載]
KeyData|臨床試験結果
📊CASPIAN試験³⁻⁵⁾ >>詳しくみる
化学療法歴のないPS 0-1のED-SCLC患者805例を対象に、DurvalumabまたはDurvalumab+Tremelimumabとプラチナ製剤併用療法比較した国際共同第Ⅲ相試験
主要評価項目 : 全生存期間 (OS)³⁾
- Durvalumab併用群 : 13.0ヵ月
- プラチナ製剤併用療法群 : 10.3ヵ月
HR 0.73 [95%CI 0.591~0.909] p=0.0047
副次評価項目 : 無増悪生存期間 (PFS)³⁾
- Durvalumab併用群 : 5.1ヵ月
- プラチナ製剤併用療法群 : 5.4ヵ月
HR 0.73 [95%CI 0.65-0.94]
更新された報告 : 18ヵ月OS率⁴⁾
- Durvalumab併用群 : 32.0%
- プラチナ製剤併用療法群 : 24.8%
HR 0.75 [95%CI : 0.62-0.91]
更新された報告 : 36ヵ月OS率⁵⁾
- Durvalumab併用群 : 17.6%
- プラチナ製剤併用療法群 : 15.8%
HR 0.71 [95%CI : 0.60-0.86]
日本人集団のサブ解析⁶⁾
- OS : HR 0.77 ([95%CI 0.26‒2.26] 未達 vs 15.2ヵ月)
- PFS : HR 0.90 ([95%CI 0.43‒1.89])
- 毒性に関して全体集団と同様の傾向
各プロトコル
以下はCASPIAN試験³⁻⁵⁾より引用
投与開始基準例
- 好中球数≧1500/mm³
- 血小板数≧100,000/mm³
- ヘモグロビン≧9.0g/dL
- 血清ビリルビン≦1.5×正常域上限(ULN)
- AST / ALT / ALP ≦2.5×ULN
肝転移時は≦5×ULN
- クレアチニンクリアランス
- シスプラチン投与 >60mL/min
- カルボプラチン投与 >45mL/min
レジメンの特徴と注意点
肺癌診療ガイドライン2025の推奨³⁾

進展型小細胞肺癌 (PS 0-1) には、 プラチナ製剤/エトポシド併用療法+PD-L1阻害薬の併用治療を行うよう強く推奨 (1A)
投与開始前の注意点
- CBDCA、CDDPによるアレルギー歴を確認。
- PSが0~1が治験時の患者登録基準である。
- 自己免疫疾患、 間質性肺疾患等の既往がある患者はirAEのリスク因子となるため投与前に事前に評価を行う。
- 4コース終了後はPD、 有害事象あるいは臨床上の利益がない状況となるまでデュルバルマブ単剤での維持療法の継続について判断が必要なことに留意する。
副作用と対策
- 本剤のT細胞活性化作用により、 過度の免疫反応に起因すると考えられる様々な疾患や病態 (irAE) が現れることがある。
- CBDCAとアミノグリコシド系抗菌薬の併用によって聴覚障害や腎毒性が増強する可能性があるため注意。
- 内分泌機能検査 (TSH、 FT4、 ACTHなど) を定期的に実施し、モニタリングする。
- その他尿検査や画像評価などの定期的なモニタリングも必要である。
- 有害事象が疑われた場合には、 各専門医へのコンサルトも検討する。
使用上のワンポイント
ED-SCLCは根治不能であり、 患者のQOL改善と生存期問延長を重視した選択が重要。 PS良好例では、 第一選択として以下の理由から白金製剤併用+ICIが挙がる。 ICIが併用できないときや、間質性肺疾患合併時にはIP療法またはPE療法が候補となる。
IP療法 (CDDP+CPT-11) が標準であった
📊JCOG9511試験
PS0~2の70歳以下を対象として、 IP療法 (CDDP+CPT-11)とPE療法 (CDDP+ETP)と比較した第Ⅲ相試験。 2回目の中間解析で有効中止され、 IP療法が優越性を示した。 OS中央値 : 12.8ヵ月 vs 9.4ヵ月。
その後、白金製剤併用+ICIが標準療法に
📊IMpower133試験
CE療法 +Atezolizumabが、 CE療法に対してOSを優位に延長した。 OS中央値 : 12.3ヵ月 vs 10.3ヵ月。
📊CASPIAN試験
PE/CE療法+Durvalumabが、 PE/CE療法に対してOSを優位に延長した。 OS中央値 : 13.0ヵ月 vs 10.3ヵ月。
ICIそれぞれの併用療法比較
1.維持療法中の投与間隔が異なる
- CASPIAN試験 : Durvalumab 4週
- IMpower133試験 : Atezolizumab 3週
2.CASPIAN試験ではCDDPの使用が可能
直接比較した臨床試験はないが、 いずれの薬剤もPD-L1阻害薬であり、 効果・副作用に関しても同様と考えられる。
出典
1) アストラゼネカ株式会社 「イミフィンジ®︎、 イジュド®︎適正使用ガイド」 (2025年9月作成) [最終閲覧 2025/10/19]
*アストラゼネカ株式会社の外部サイトへ遷移します
2) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2025年10月19日
HOKUTO編集部医師監修
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。




