GC + Nivolumab
ゲムシタビン+シスプラチン+ニボルマブ
2023年12月18日に尿路上皮癌の1次治療 (化学療法を併用) の効能追加を申請。 2024年12月6日の二部会で報告、 2024年12月27日に正式承認となった。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒト型抗ヒトPD-1モノクローナル抗体 ニボルマブ
*小野薬品工業の外部サイトへ遷移します
- ジェムザール®など (添付文書³⁾/適正使用情報⁴⁾*)
抗悪性腫瘍薬 > 代謝拮抗薬 ゲムシタビン
*日本イーライリリーの外部サイトへ遷移します
抗悪性腫瘍薬 > 白金製剤 シスプラチン
*日本化薬の外部サイトへ遷移します
投与スケジュール
CheckMate 901試験のプロトコル⁷⁾
1~6サイクル目

ニボルマブ360mgとシスプラチン70mg/m²をDay1に、 ゲムシタビン1000mg/m²をDay1,8に投与、 3週サイクルで最大6サイクル実施。
※先にニボルマブを30分以上かけて点滴静注し、 投与完了後、 30分以上間隔をあけて化学療法を実施。
7サイクル目以降 (最長2年間)
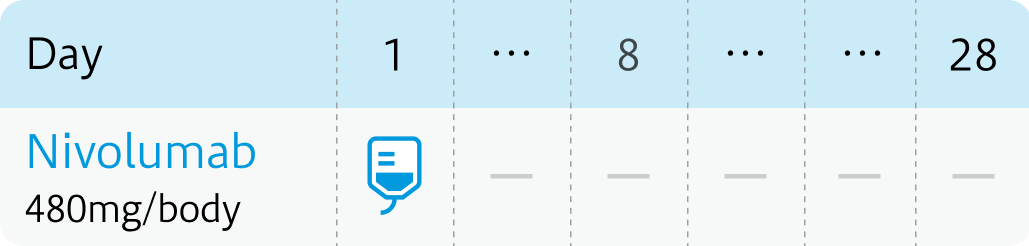
本邦添付文書にはニボルマブ維持療法は1回240mgを2週間間隔の記載もあり。
その後、 ニボルマブ480mgを4週毎の単独維持療法に移行し、 最長2年間投与する。
N Engl J Med. 2023;389(19):1778-89.より作図
特徴と注意点
CheckMate 901試験の結果、 CCr≧60ml/minで、 周術期化学療法終了から12ヵ月以上経過し、 局所進行/転移性尿路上皮癌であれば、 GC療法単独 (GEM+CDDP) より本レジメンの方が、 PFS、 OSともに優れていた⁷⁾。
今後、 EV+Pembrolizumabと同様、 1次治療の重要なオプションとなり、 特にEVの皮疹や神経障害、 高血糖などを憂慮する場合に本レジメンが勧められる可能性がある (2024年12月6日の二部会で承認了承、 今後正式承認見込み)。
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
KeyData|臨床試験結果
CheckMate 901試験
N Engl J Med. 2023;389(19):1778-89.⁷⁾
未治療の切除不能または転移性尿路上皮癌患者を対象に、 GC療法とニボルマブの併用療法の有効性および安全性について、 GC単独療法を対照として比較検討した第Ⅲ相ランダム化比較試験。 主要評価項目は、 全生存期間 (OS) と無増悪生存期間 (PFS) であった。 (対象は608例でGC+Nivo群 304例、GC療法群 304例)
2つのパートに分かれており、 第1部では、 GC+Nivo群の併用療法とGC療法群に割り付けられ、 第2部では、 NIVO+イピリムマブまたはプラチナ製剤ベースの化学療法を受ける群に割り付けられた。 以下は第1部の結果。
有効性|GC+Nivo群
追跡期間中央値 : 33.6ヵ月
- mOS : 21.7ヵ月 (95%CI 18.6-26.4ヵ月)
GC療法群 : 18.9ヵ月(95%CI 14.7-22.4ヵ月)
HR 0.78 (95%CI 0.63-0.96)、 p=0.0171
- OS率 : 12ヵ月 70.2% → 24ヵ月 46.9%
GC療法群 : 62.7% → 40.7%
- mPFS : 7.9ヵ月 (95%CI 7.6-9.5ヵ月)
GC療法群 : 7.6ヵ月 (95%CI 6.1-7.8ヵ月)
HR 0.72 (95%CI 0.59-0.88)、 p=0.0012
- PFS率 : 12ヵ月 34.2% → 24ヵ月 23.5%
GC療法群 : 21.8% → 9.6%
- ORR : 57.6% (95%CI 51.8–63.2%)
GC療法群 : 43.1% (95%CI 37.5–48.9%)
安全性|AE発現
- ≧Grade3の治療関連AE、 免疫関連AE
GC+Nivo群 : 61.8%、 6.6%
GC療法群 : 51.7%、 0%
出典
1) 小野薬品工業株式会社. オプジーボ®電子添文 (2024年12月改訂第22版) [最終閲覧 : 2025/1/24]
2) 小野薬品工業株式会社. オプジーボ®適正使用ガイド (2024年12月作成) [最終閲覧 : 2025/1/24]
3) 日本イーライリリー. ジェムザール®電子添文 (2024年12月改訂 第2版) [最終閲覧 : 2025/1/24]
4) 日本イーライリリー. ジェムザール®適正使用ガイド (2024年6月作成) [最終閲覧 : 2025/1/24]
5) 日本化薬. ランダ®電子添文 (2024年12月改訂 第3版) [最終閲覧 : 2025/1/24]
6) 日本化薬. ランダ®安全性情報 (2021年6月作成) [最終閲覧 : 2025/1/24]
最終更新 : 2025年1月24日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
GC + Nivolumab
2023年12月18日に尿路上皮癌の1次治療 (化学療法を併用) の効能追加を申請。 2024年12月6日の二部会で報告、 2024年12月27日に正式承認となった。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒト型抗ヒトPD-1モノクローナル抗体 ニボルマブ
*小野薬品工業の外部サイトへ遷移します
- ジェムザール®など (添付文書³⁾/適正使用情報⁴⁾*)
抗悪性腫瘍薬 > 代謝拮抗薬 ゲムシタビン
*日本イーライリリーの外部サイトへ遷移します
抗悪性腫瘍薬 > 白金製剤 シスプラチン
*日本化薬の外部サイトへ遷移します
投与スケジュール
CheckMate 901試験のプロトコル⁷⁾
1~6サイクル目

ニボルマブ360mgとシスプラチン70mg/m²をDay1に、 ゲムシタビン1000mg/m²をDay1,8に投与、 3週サイクルで最大6サイクル実施。
※先にニボルマブを30分以上かけて点滴静注し、 投与完了後、 30分以上間隔をあけて化学療法を実施。
7サイクル目以降 (最長2年間)

本邦添付文書にはニボルマブ維持療法は1回240mgを2週間間隔の記載もあり。
その後、 ニボルマブ480mgを4週毎の単独維持療法に移行し、 最長2年間投与する。
N Engl J Med. 2023;389(19):1778-89.より作図
特徴と注意点
CheckMate 901試験の結果、 CCr≧60ml/minで、 周術期化学療法終了から12ヵ月以上経過し、 局所進行/転移性尿路上皮癌であれば、 GC療法単独 (GEM+CDDP) より本レジメンの方が、 PFS、 OSともに優れていた⁷⁾。
今後、 EV+Pembrolizumabと同様、 1次治療の重要なオプションとなり、 特にEVの皮疹や神経障害、 高血糖などを憂慮する場合に本レジメンが勧められる可能性がある (2024年12月6日の二部会で承認了承、 今後正式承認見込み)。
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
KeyData|臨床試験結果
CheckMate 901試験
N Engl J Med. 2023;389(19):1778-89.⁷⁾
未治療の切除不能または転移性尿路上皮癌患者を対象に、 GC療法とニボルマブの併用療法の有効性および安全性について、 GC単独療法を対照として比較検討した第Ⅲ相ランダム化比較試験。 主要評価項目は、 全生存期間 (OS) と無増悪生存期間 (PFS) であった。 (対象は608例でGC+Nivo群 304例、GC療法群 304例)
2つのパートに分かれており、 第1部では、 GC+Nivo群の併用療法とGC療法群に割り付けられ、 第2部では、 NIVO+イピリムマブまたはプラチナ製剤ベースの化学療法を受ける群に割り付けられた。 以下は第1部の結果。
有効性|GC+Nivo群
追跡期間中央値 : 33.6ヵ月
- mOS : 21.7ヵ月 (95%CI 18.6-26.4ヵ月)
GC療法群 : 18.9ヵ月(95%CI 14.7-22.4ヵ月)
HR 0.78 (95%CI 0.63-0.96)、 p=0.0171
- OS率 : 12ヵ月 70.2% → 24ヵ月 46.9%
GC療法群 : 62.7% → 40.7%
- mPFS : 7.9ヵ月 (95%CI 7.6-9.5ヵ月)
GC療法群 : 7.6ヵ月 (95%CI 6.1-7.8ヵ月)
HR 0.72 (95%CI 0.59-0.88)、 p=0.0012
- PFS率 : 12ヵ月 34.2% → 24ヵ月 23.5%
GC療法群 : 21.8% → 9.6%
- ORR : 57.6% (95%CI 51.8–63.2%)
GC療法群 : 43.1% (95%CI 37.5–48.9%)
安全性|AE発現
- ≧Grade3の治療関連AE、 免疫関連AE
GC+Nivo群 : 61.8%、 6.6%
GC療法群 : 51.7%、 0%
出典
1) 小野薬品工業株式会社. オプジーボ®電子添文 (2024年12月改訂第22版) [最終閲覧 : 2025/1/24]
2) 小野薬品工業株式会社. オプジーボ®適正使用ガイド (2024年12月作成) [最終閲覧 : 2025/1/24]
3) 日本イーライリリー. ジェムザール®電子添文 (2024年12月改訂 第2版) [最終閲覧 : 2025/1/24]
4) 日本イーライリリー. ジェムザール®適正使用ガイド (2024年6月作成) [最終閲覧 : 2025/1/24]
5) 日本化薬. ランダ®電子添文 (2024年12月改訂 第3版) [最終閲覧 : 2025/1/24]
6) 日本化薬. ランダ®安全性情報 (2021年6月作成) [最終閲覧 : 2025/1/24]
最終更新 : 2025年1月24日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。