基底細胞癌
Basal cell carcinoma
監修 : 国立がん研究センター中央 皮膚腫瘍科 並川健二郎先生
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
基底細胞癌の疫学
表皮基底細胞や毛芽細胞に類似した腫瘍細胞で構成される皮膚がんの一種
基底細胞癌は、 表皮基底細胞や毛芽細胞に類似した腫瘍細胞で構成される皮膚がんの一種であり、 毛包上皮の基底細胞を起源とする可能性が指摘されている。 顔面の中央部をはじめとした頭頚部領域に好発することから、 日光紫外線曝露が発症に関与していると考えられている。 また、 PTCH1遺伝子やSMO遺伝子の変異によるヘッジホッグシグナル伝達経路の活性化も発症に関与していると考えられている。 高齢者に多いが、 色素性乾皮症や基底細胞母斑症候群では若年でも発症する。
皮膚がん全体の37.2%を占める
アジア人の基底細胞癌の罹患率は白人より圧倒的に低いものの、 わが国の全国がん登録データでは皮膚がん全体の37.2%を占めており、 年齢調整罹患率はWHOモデルで10万人あたり3.63と最も頻度が高い皮膚がんである¹⁾。 また、 白人の基底細胞癌は無色素性で境界不明瞭であることが多いのに対し、 アジア人の基底細胞癌は色素性で境界明瞭であることが多い。
基底細胞癌の分類
基底細胞癌の病理組織学的分類
低リスク型基底細胞癌
- 結節型 (nodular)
- 表在型 (superficial)
高リスク型基底細胞癌
- 斑状強皮症/硬化型 (morpheic/sclerosing)
- 微小結節型 (micronodular)
- 浸潤型 (infiltrative)
- 基底有棘細胞型 (basosquamous)
- 癌肉腫様型 (carcinosarcomatous)
TNM分類については、 わが国では便宜上UICC第8版の皮膚がん分類が用いられるが、 基底細胞癌はリンパ節や遠隔臓器への転移が極めて稀であるため、 臨床現場ではあまり活用されていない。
基底細胞癌の治療
切除可能な場合
外科的切除が第一選択であり、 完全切除が得られれば治癒が見込める。
手術が適さない場合
整容性や機能面での考慮が必要な症例では、 薬物療法が選択肢となる。
▼イミキモド外用療法について
日本では基底細胞癌に対する適応はない。
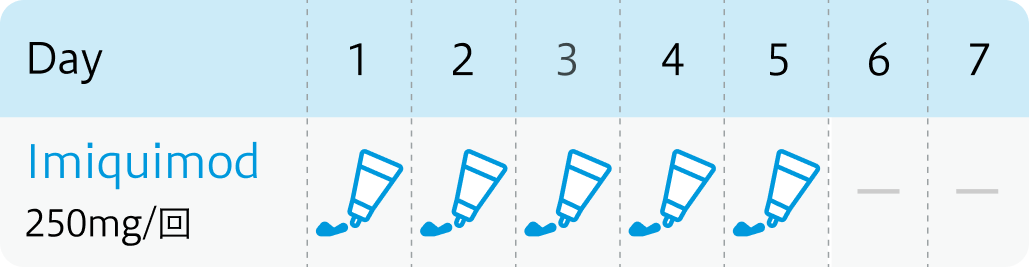
FDA (アメリカ食品医薬品局) の推奨用量 最大1包 (250mg イミキモドとして12.5mg) まで1日1回、 週5回塗布する。 6週間を1コースとし、その後経過観察を行う。
Vehicle controlとの比較試験
表在型基底細胞癌の患者を対象としたランダム化第III相試験で、 イミキモド週5回投与群185例の病変消失割合は病理学的評価で82%、 臨床的評価と病理学的評価を合わせると75%と報告されている²⁾。
他の治療法との比較試験
表在型基底細胞癌の患者を対象に、 光線力学的療法 (PDT) 群292例、 イミキモド外用療法群198例、 5-FU外用療法群201例のいずれかに無作為に割り付けた。 病理学的腫瘍消失割合は、 PDT群73%、 イミキモド外用療法群83%、 5-FU外用療法群80%と報告され、 イミキモド外用療法が最も優れていた³⁾。
同試験のフォローアップでは、 5年無局所再発生存割合がPDT群63%、 イミキモド外用療法群81%、 5-FU外用療法群70%と報告され、 長期成績でもイミキモド外用療法が最も優れていた⁴⁾。
局所進行性・転移性基底細胞癌
進行性または遠隔転移を有する基底細胞癌は、 全身化学療法が適応となる。 従来はシスプラチンを含むレジメン CA (CDDP+Doxorubicin、 C'A' (CBDCA+Epirubicin)、 FP (5-FU+CDDP)などが有棘細胞癌に準じて用いられてきた。 近年、 ヘッジホッグ経路を標的とした治療薬として、 vismodegibおよびsonidegibが海外で承認されているが、 日本では未承認である。
▼セミプリマブ療法について
日本では基底細胞癌に対する適応はない。 抗PD-1抗体のセミプリマブが米国FDAに承認されており、 ヘッジホッグ経路阻害薬に不応の局所進行性または転移性基底細胞癌の患者を対象とした第II相試験で、 奏効割合が局所進行性84例で31%⁵⁾、 転移性54例で22%と報告されている⁶⁾
▼ニボルマブ療法
根治切除不能な進行・再発の上皮系皮膚悪性腫瘍の患者を対象に、 ニボルマブ単独療法の有効性を評価する国内第II相試験が行われた。
2週間間隔の場合
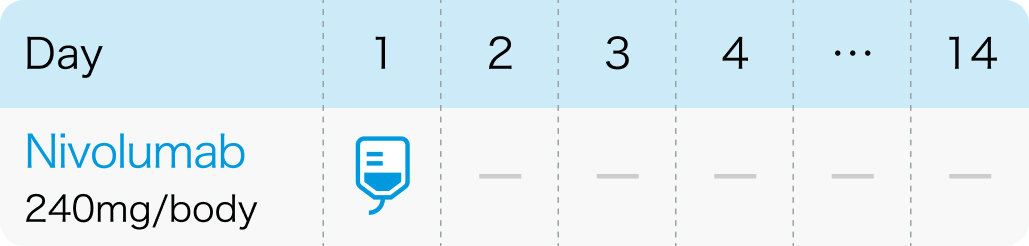
または 4週間間隔の場合

上皮系皮膚悪性腫瘍患者31名 (有棘細胞癌20名、 基底細胞癌2名、 乳房外パジェット病4名、 皮膚付属器癌5名 [エクリン汗孔癌3名、 汗腺癌1名、 皮膚粘液癌1名]) の奏効割合は19.4% (基底細胞癌は50.0%) と報告された。
この結果より、 日本では2024年2月にニボルマブが根治切除不能な進行・再発の上皮系皮膚悪性腫瘍に対し承認されている⁷⁾。
出典
1) Ogata D, et al. Cancer Sci 2023;114:2986-92.
2) Geisse J, et al. J Am Acad Dermatol. 2004;50(5):722-33.
3) Arits AH, et al. Lancet Oncol. 2013;14(7):647-54.
4) Jansen MHE, et al. J Invest Dermatol. 2018;138(3):527-33.
5) Stratigos A, et al. Lancet Oncol 2021;22:848-857.
6) Lewis KD, et al. Ann Oncol 2024;35:221-228.
7) 最適使用推進ガイドライン ニボルマブ (遺伝子組換え) ~上皮系皮膚悪性腫瘍~
最終更新日 : 2025年3月5日
監修医師 : 国立がん研究センター中央病院 皮膚腫瘍科 医長 並川 健二郎先生
基底細胞癌
監修 : 国立がん研究センター中央 皮膚腫瘍科 並川健二郎先生
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
基底細胞癌の疫学
表皮基底細胞や毛芽細胞に類似した腫瘍細胞で構成される皮膚がんの一種
基底細胞癌は、 表皮基底細胞や毛芽細胞に類似した腫瘍細胞で構成される皮膚がんの一種であり、 毛包上皮の基底細胞を起源とする可能性が指摘されている。 顔面の中央部をはじめとした頭頚部領域に好発することから、 日光紫外線曝露が発症に関与していると考えられている。 また、 PTCH1遺伝子やSMO遺伝子の変異によるヘッジホッグシグナル伝達経路の活性化も発症に関与していると考えられている。 高齢者に多いが、 色素性乾皮症や基底細胞母斑症候群では若年でも発症する。
皮膚がん全体の37.2%を占める
アジア人の基底細胞癌の罹患率は白人より圧倒的に低いものの、 わが国の全国がん登録データでは皮膚がん全体の37.2%を占めており、 年齢調整罹患率はWHOモデルで10万人あたり3.63と最も頻度が高い皮膚がんである¹⁾。 また、 白人の基底細胞癌は無色素性で境界不明瞭であることが多いのに対し、 アジア人の基底細胞癌は色素性で境界明瞭であることが多い。
基底細胞癌の分類
基底細胞癌の病理組織学的分類
低リスク型基底細胞癌
- 結節型 (nodular)
- 表在型 (superficial)
高リスク型基底細胞癌
- 斑状強皮症/硬化型 (morpheic/sclerosing)
- 微小結節型 (micronodular)
- 浸潤型 (infiltrative)
- 基底有棘細胞型 (basosquamous)
- 癌肉腫様型 (carcinosarcomatous)
TNM分類については、 わが国では便宜上UICC第8版の皮膚がん分類が用いられるが、 基底細胞癌はリンパ節や遠隔臓器への転移が極めて稀であるため、 臨床現場ではあまり活用されていない。
基底細胞癌の治療
切除可能な場合
外科的切除が第一選択であり、 完全切除が得られれば治癒が見込める。
手術が適さない場合
整容性や機能面での考慮が必要な症例では、 薬物療法が選択肢となる。
▼イミキモド外用療法について
日本では基底細胞癌に対する適応はない。

FDA (アメリカ食品医薬品局) の推奨用量 最大1包 (250mg イミキモドとして12.5mg) まで1日1回、 週5回塗布する。 6週間を1コースとし、その後経過観察を行う。
Vehicle controlとの比較試験
表在型基底細胞癌の患者を対象としたランダム化第III相試験で、 イミキモド週5回投与群185例の病変消失割合は病理学的評価で82%、 臨床的評価と病理学的評価を合わせると75%と報告されている²⁾。
他の治療法との比較試験
表在型基底細胞癌の患者を対象に、 光線力学的療法 (PDT) 群292例、 イミキモド外用療法群198例、 5-FU外用療法群201例のいずれかに無作為に割り付けた。 病理学的腫瘍消失割合は、 PDT群73%、 イミキモド外用療法群83%、 5-FU外用療法群80%と報告され、 イミキモド外用療法が最も優れていた³⁾。
同試験のフォローアップでは、 5年無局所再発生存割合がPDT群63%、 イミキモド外用療法群81%、 5-FU外用療法群70%と報告され、 長期成績でもイミキモド外用療法が最も優れていた⁴⁾。
局所進行性・転移性基底細胞癌
進行性または遠隔転移を有する基底細胞癌は、 全身化学療法が適応となる。 従来はシスプラチンを含むレジメン CA (CDDP+Doxorubicin、 C'A' (CBDCA+Epirubicin)、 FP (5-FU+CDDP)などが有棘細胞癌に準じて用いられてきた。 近年、 ヘッジホッグ経路を標的とした治療薬として、 vismodegibおよびsonidegibが海外で承認されているが、 日本では未承認である。
▼セミプリマブ療法について
日本では基底細胞癌に対する適応はない。 抗PD-1抗体のセミプリマブが米国FDAに承認されており、 ヘッジホッグ経路阻害薬に不応の局所進行性または転移性基底細胞癌の患者を対象とした第II相試験で、 奏効割合が局所進行性84例で31%⁵⁾、 転移性54例で22%と報告されている⁶⁾
▼ニボルマブ療法
根治切除不能な進行・再発の上皮系皮膚悪性腫瘍の患者を対象に、 ニボルマブ単独療法の有効性を評価する国内第II相試験が行われた。
2週間間隔の場合

または 4週間間隔の場合

上皮系皮膚悪性腫瘍患者31名 (有棘細胞癌20名、 基底細胞癌2名、 乳房外パジェット病4名、 皮膚付属器癌5名 [エクリン汗孔癌3名、 汗腺癌1名、 皮膚粘液癌1名]) の奏効割合は19.4% (基底細胞癌は50.0%) と報告された。
この結果より、 日本では2024年2月にニボルマブが根治切除不能な進行・再発の上皮系皮膚悪性腫瘍に対し承認されている⁷⁾。
出典
1) Ogata D, et al. Cancer Sci 2023;114:2986-92.
2) Geisse J, et al. J Am Acad Dermatol. 2004;50(5):722-33.
3) Arits AH, et al. Lancet Oncol. 2013;14(7):647-54.
4) Jansen MHE, et al. J Invest Dermatol. 2018;138(3):527-33.
5) Stratigos A, et al. Lancet Oncol 2021;22:848-857.
6) Lewis KD, et al. Ann Oncol 2024;35:221-228.
7) 最適使用推進ガイドライン ニボルマブ (遺伝子組換え) ~上皮系皮膚悪性腫瘍~
最終更新日 : 2025年3月5日
監修医師 : 国立がん研究センター中央病院 皮膚腫瘍科 医長 並川 健二郎先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。




