Pembrolizumab (KEYNOTE-522)
ペムブロリズマブ (キイトルーダ®)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PD-1モノクローナル抗体 ペムブロリズマブ (遺伝子組換え)
*MSD株式会社の外部サイトへ遷移します
投与スケジュール
KEYNOTE-522¹⁾²⁾ : ホルモン受容体陰性かつHER2陰性再発高リスク乳癌の術前・術後療法
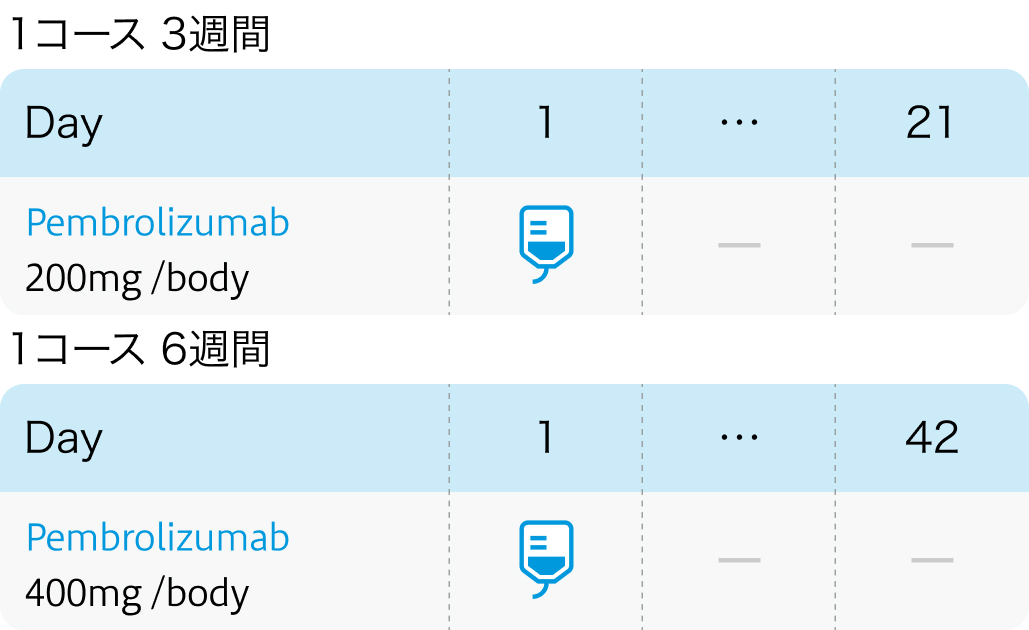
KEYNOTE-522試験では、術前療法としてペムブロリズマブ200mg 3週間間隔投与と化学療法を併用し、 術後療法としてペムブロリズマブ200mg 3週間間隔投与を9コース投与した。
本邦の添付文書上は6週間隔投与も可能
なお、 添付文書上は6週間隔投与も可能。 投与回数は3週間間隔投与の場合、 術後薬物療法は9回まで、 6週間間隔投与の場合、 術後薬物療法は5回までとする。
各プロトコル
投与開始基準
KEYNOTE-522¹⁾²⁾ : 前治療歴のないトリプルネガティブ乳癌でPS0、1の以下に該当する患者 (一部抜粋)

休薬・中止・減量基準

特徴と注意点
ホルモン受容体陰性かつHER2陰性で再発高リスクの乳癌における術後薬物療法としてペムブロリズマブ単剤で投与する。
- 1回200mgを3週間間隔または、 1回400mgを6週間間隔で30分間かけて点滴静注する。
- 投与回数は3週間間隔投与の場合、 術後薬物療法は9回まで、 6週間間隔投与の場合、 術後薬物療法は5回までとする。
- 免疫チェックポイント阻害薬の有害事象は多岐にわたり、 発現時期も明確でないため、 患者の体調変化のチェックを注意深くする必要がある。
- ペムブロリズマブ投与時は、 インラインフィルター (0.2~5μm) を使用する。
関連する臨床試験
KEYNOTE-522試験¹⁾²⁾
早期トリプルネガティブ乳癌患者において、 術前ペムブロリズマブと化学療法の併用+術後ペムブロリズマブ投与の効果を、 術前化学療法単独を対照に検証した第Ⅲ相二重盲検ランダム化比較試験KEYNOTE-522の結果より、 病理学的完全奏効 (pCR) 率と無イベント生存期間 (EFS) を有意に改善させることが示された。
主な有害事象
一部引用 (カッコ内は≧Grade3)
- 貧血 54.8% (18.0%)
- 好中球減少症 46.9% (34.5%)
- ALT上昇 26.1% (5.5%)
- 好中球数減少 23.6% (18.6%)
- AST上昇 20.1% (2.6%)
- 悪心 63.2% (3.4%)
- 脱毛症 60.2% (0%)
- 倦怠感 42.1% (3.6%)
- 下痢 30.4% (2.6%)
- 嘔吐 25.5% (2.4%)
- 便秘 24.0% (0%)
pCR率 (ypT0/Tis ypN0)
追跡期間中央値 : 15.5ヵ月
- ペムブロリズマブ群 : 64.8%
(95%CI 59.9-69.5%)
- プラセボ群 : 51.2%
(95%CI 44.1-58.3%)
p<0.001
サブグループ解析
PD-L1発現を含め、 事前規定された全サブグループにおいて、 ペムブロリズマブ群のプラセボ群に対する優位性が概ね一貫して認められた。
EFS
追跡期間中央値 : 39.1ヵ月
イベント数
- ペムブロリズマブ群 : 123例
- プラセボ群 : 93例
HR 0.63、 (95%CI 0.48-0.82)、 p<0.001
EFS率 (36ヵ月時)
- ペムブロリズマブ群 : 84.5%
(95%CI 81.7-86.9%)
- プラセボ群 : 76.8%
(95%CI 72.2-80.7%)
サブグループ解析
PD-L1発現およびリンパ節転移の数を含め、 事前に規定された全てのサブグループにおいて、 ペムブロリズマブ群のプラセボ群に対する優位性が概ね一貫して認められた。
pCR率 (ypT0 ypN0)
- ペムブロリズマブ群 : 59.9%
(95%CI 54.9-64.7%)
- プラセボ群 : 45.3%
(95%CI 38.3-52.4%)
pCR率 (ypT0/Tis)
- ペムブロリズマブ群 : 68.6%
(95%CI 63.8-73.1%)
- プラセボ群 : 53.7%
(95%CI 46.6-60.8%)
PD-L1陽性患者のpCR率 (ypT0/Tis ypN0)
- ペムブロリズマブ群 : 68.9%
- プラセボ群 : 54.9%
PD-L1陰性患者のpCR率 (ypT0/Tis ypN0)
- ペムブロリズマブ群 : 45.3%
- プラセボ群 : 30.3%
OS
追跡期間中央値 : 39.1ヵ月
イベント数
- ペムブロリズマブ群 : 80例
- プラセボ群 : 55例
HR 0.72、 (95%CI 0.51-1.02)
OS率 (36ヵ月時)
- ペムブロリズマブ群 : 89.7%
(95%CI 87.3-91.7%)
- プラセボ群 : 86.9%
(95%CI 83.0-89.9%)
出典
- Pembrolizumab for Early Triple-Negative Breast Cancer. N Engl J Med. 2020 Feb 27;382(9):810-821. PMID: 32101663
- Event-free Survival with Pembrolizumab in Early Triple-Negative Breast Cancer. N Engl J Med. 2022 Feb 10;386(6):556-567. PMID: 35139274
最終更新日 : 2025年8月6日
監修医師 : HOKUTO編集部監修医師
執筆 : 公益財団法人 がん研究会 がん研有明病院 薬剤部 平岡 知子先生
Pembrolizumab (KEYNOTE-522)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PD-1モノクローナル抗体 ペムブロリズマブ (遺伝子組換え)
*MSD株式会社の外部サイトへ遷移します
投与スケジュール
KEYNOTE-522¹⁾²⁾ : ホルモン受容体陰性かつHER2陰性再発高リスク乳癌の術前・術後療法

KEYNOTE-522試験では、術前療法としてペムブロリズマブ200mg 3週間間隔投与と化学療法を併用し、 術後療法としてペムブロリズマブ200mg 3週間間隔投与を9コース投与した。
本邦の添付文書上は6週間隔投与も可能
なお、 添付文書上は6週間隔投与も可能。 投与回数は3週間間隔投与の場合、 術後薬物療法は9回まで、 6週間間隔投与の場合、 術後薬物療法は5回までとする。
各プロトコル
投与開始基準
KEYNOTE-522¹⁾²⁾ : 前治療歴のないトリプルネガティブ乳癌でPS0、1の以下に該当する患者 (一部抜粋)

休薬・中止・減量基準

特徴と注意点
ホルモン受容体陰性かつHER2陰性で再発高リスクの乳癌における術後薬物療法としてペムブロリズマブ単剤で投与する。
- 1回200mgを3週間間隔または、 1回400mgを6週間間隔で30分間かけて点滴静注する。
- 投与回数は3週間間隔投与の場合、 術後薬物療法は9回まで、 6週間間隔投与の場合、 術後薬物療法は5回までとする。
- 免疫チェックポイント阻害薬の有害事象は多岐にわたり、 発現時期も明確でないため、 患者の体調変化のチェックを注意深くする必要がある。
- ペムブロリズマブ投与時は、 インラインフィルター (0.2~5μm) を使用する。
関連する臨床試験
KEYNOTE-522試験¹⁾²⁾
早期トリプルネガティブ乳癌患者において、 術前ペムブロリズマブと化学療法の併用+術後ペムブロリズマブ投与の効果を、 術前化学療法単独を対照に検証した第Ⅲ相二重盲検ランダム化比較試験KEYNOTE-522の結果より、 病理学的完全奏効 (pCR) 率と無イベント生存期間 (EFS) を有意に改善させることが示された。
主な有害事象
一部引用 (カッコ内は≧Grade3)
- 貧血 54.8% (18.0%)
- 好中球減少症 46.9% (34.5%)
- ALT上昇 26.1% (5.5%)
- 好中球数減少 23.6% (18.6%)
- AST上昇 20.1% (2.6%)
- 悪心 63.2% (3.4%)
- 脱毛症 60.2% (0%)
- 倦怠感 42.1% (3.6%)
- 下痢 30.4% (2.6%)
- 嘔吐 25.5% (2.4%)
- 便秘 24.0% (0%)
pCR率 (ypT0/Tis ypN0)
追跡期間中央値 : 15.5ヵ月
- ペムブロリズマブ群 : 64.8%
(95%CI 59.9-69.5%)
- プラセボ群 : 51.2%
(95%CI 44.1-58.3%)
p<0.001
サブグループ解析
PD-L1発現を含め、 事前規定された全サブグループにおいて、 ペムブロリズマブ群のプラセボ群に対する優位性が概ね一貫して認められた。
EFS
追跡期間中央値 : 39.1ヵ月
イベント数
- ペムブロリズマブ群 : 123例
- プラセボ群 : 93例
HR 0.63、 (95%CI 0.48-0.82)、 p<0.001
EFS率 (36ヵ月時)
- ペムブロリズマブ群 : 84.5%
(95%CI 81.7-86.9%)
- プラセボ群 : 76.8%
(95%CI 72.2-80.7%)
サブグループ解析
PD-L1発現およびリンパ節転移の数を含め、 事前に規定された全てのサブグループにおいて、 ペムブロリズマブ群のプラセボ群に対する優位性が概ね一貫して認められた。
pCR率 (ypT0 ypN0)
- ペムブロリズマブ群 : 59.9%
(95%CI 54.9-64.7%)
- プラセボ群 : 45.3%
(95%CI 38.3-52.4%)
pCR率 (ypT0/Tis)
- ペムブロリズマブ群 : 68.6%
(95%CI 63.8-73.1%)
- プラセボ群 : 53.7%
(95%CI 46.6-60.8%)
PD-L1陽性患者のpCR率 (ypT0/Tis ypN0)
- ペムブロリズマブ群 : 68.9%
- プラセボ群 : 54.9%
PD-L1陰性患者のpCR率 (ypT0/Tis ypN0)
- ペムブロリズマブ群 : 45.3%
- プラセボ群 : 30.3%
OS
追跡期間中央値 : 39.1ヵ月
イベント数
- ペムブロリズマブ群 : 80例
- プラセボ群 : 55例
HR 0.72、 (95%CI 0.51-1.02)
OS率 (36ヵ月時)
- ペムブロリズマブ群 : 89.7%
(95%CI 87.3-91.7%)
- プラセボ群 : 86.9%
(95%CI 83.0-89.9%)
出典
- Pembrolizumab for Early Triple-Negative Breast Cancer. N Engl J Med. 2020 Feb 27;382(9):810-821. PMID: 32101663
- Event-free Survival with Pembrolizumab in Early Triple-Negative Breast Cancer. N Engl J Med. 2022 Feb 10;386(6):556-567. PMID: 35139274
最終更新日 : 2025年8月6日
監修医師 : HOKUTO編集部監修医師
執筆 : 公益財団法人 がん研究会 がん研有明病院 薬剤部 平岡 知子先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。