MSI/MMR
提供:MSD株式会社
記載されている各薬剤及び診断薬の詳細については、 最新の電子添文をご確認ください。 また、 承認されたコンパニオン診断薬等の最新情報については、 こちらをご確認ください。

アドバイザー : 国立がん研究センター中央病院 病理診断科 科長 谷田部 恭 先生、 国立がん研究センター東病院 遺伝子診療部門 部門長 桑田 健 先生
高頻度マイクロサテライト不安定性 (MSI-High) /ミスマッチ修復機能欠損 (dMMR) の概要
MSI/MMRとは¹⁾
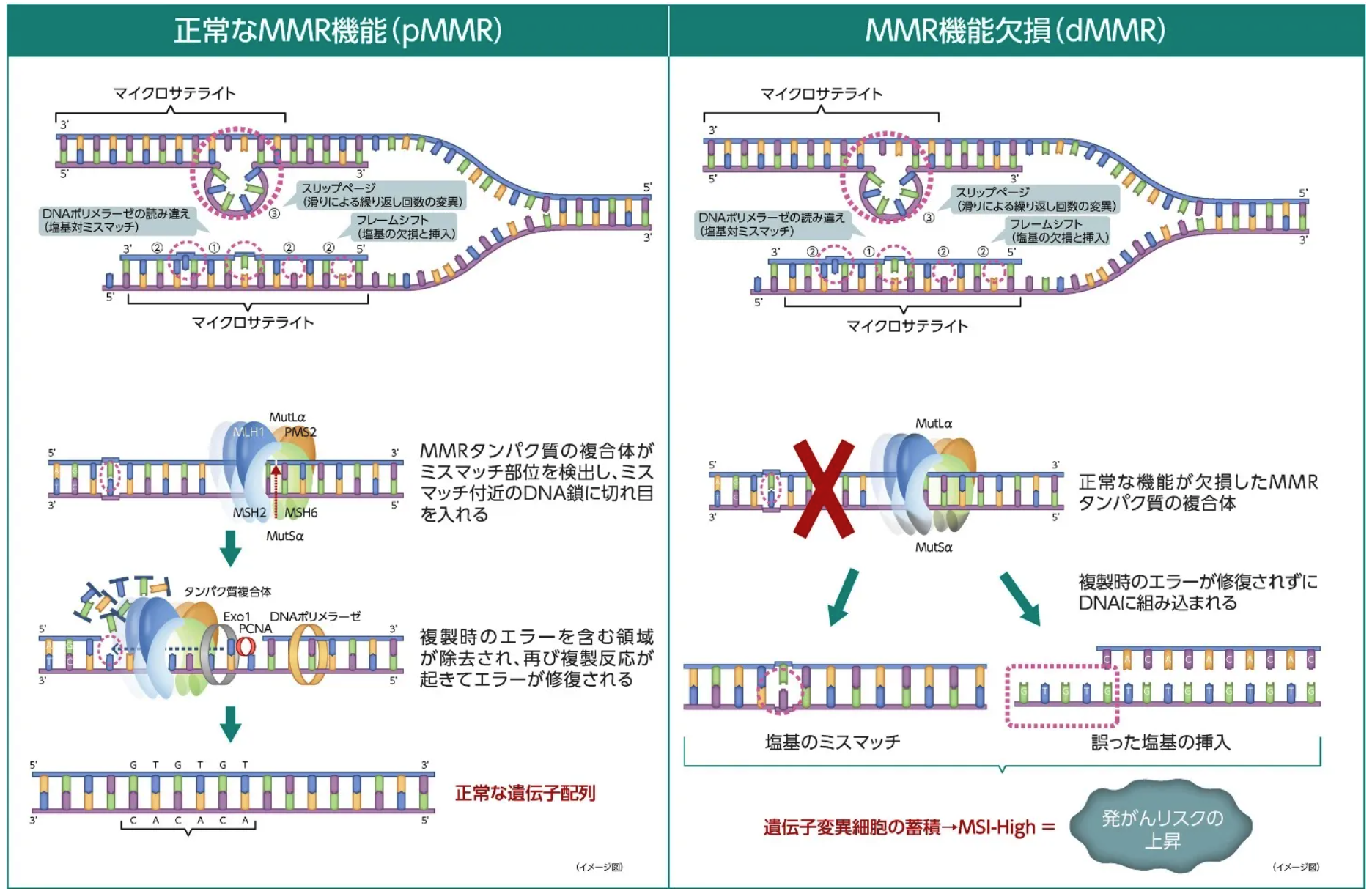
通常、 DNA複製時のエラーはミスマッチ修復 (MMR) タンパク質の複合体の機能などによって正常に修復されるが、 MMR機能が欠損するとエラーが修復されず、 マイクロサテライトが通常と異なる反復回数を示すことがある。 これをマイクロサテライト不安定性 (MSI) という。

MMR機能欠損によるMSI-High/dMMR固形がんの発症³⁻⁶⁾
MMR機能が正常な状態をpMMR (proficient MMR) といい、 MMR機能が欠損した状態をdMMR (deficient MMR) という。 MMR機能が欠損した状態ではDNA複製エラーが修復されず、 がん抑制遺伝子のフレームシフト変異などが引き起こされ、 エラーを持ったままの細胞が増殖して高頻度マイクロサテライト不安定性 (MSI-High) となり、 がん化の原因となる (MSI-High/dMMR固形がん)。
引用文献
1) Weinberg BA et al. Clin Advances Hem Onc 2019; 17: 109-119.
2) Salem ME et al. Mol Cancer Res 2018; 16: 805-812.
3) 川平正博他. 腫瘍内科 2017; 20: 325-330.
4) Li SKH et al. Trends Mol Med 2016; 287-289.
5) 前原喜彦他. Cancer Frontier 2001; 3: 119-127.
6) 菅井有他. 日本臨牀 2011; 69: 84:93.
効果予測バイオマーカーとしてのMSI-High/dMMR
MSI-High/dMMRと免疫応答
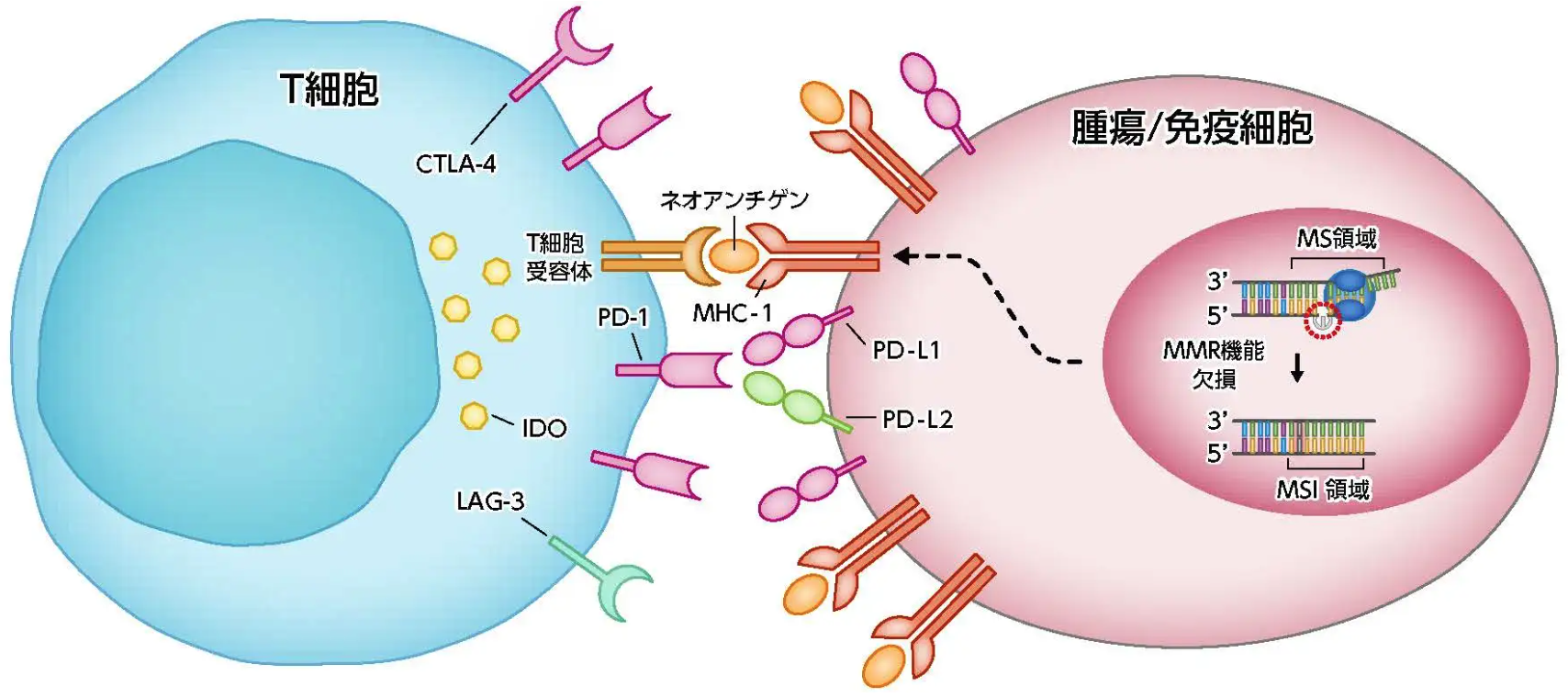
MSI-High/dMMR固形がんでは、 MMR機能の欠損により、 MSS/pMMR固形がんと比べてより多くの体細胞遺伝子変異を有することが報告されている¹⁾²⁾。 それにより腫瘍特異抗原 (ネオアンチゲン) の発現が高くなり、 T細胞の認識を受けやすくなることで、 抗PD-1抗体療法の反応性が高まると考えられている³⁾。

引用文献
1) Dubley JC et al. Clin Cancer Res 2016; 22: 813-820.
2) Le DT et al. Science 2017; 357: 409-413. 本試験で使用した治験薬はMSD社より提供された。 MSD社は投稿前の本試験のプロトコール及び最終原稿をレビューした。 Dung T. LeはMSD社よりコンサルタント料を受領している。 Aleksandra D. Eyring、 Bao H. Lam、 Andrew Joe、 S. Peter KangはMSD社の社員である。
3) Boyiadzis MM et al. J Immunother Cancer 2018; 6: 35. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
4) Llosa NJ et al. Cancer Discov 2015; 5: 43-51.
5) Pardoll DM et al. Nat Rev Cancer 2012; 12: 252-264.
MSI-High/dMMRとPD-1阻害剤の有効性
MSI-High/dMMRを有する腫瘍とPD-1阻害剤の有効性については、 KEYNOTE-158試験及びKEYNOTE-177試験において検討された。
●KEYNOTE-158試験 (固形がんを対象としたペムブロリズマブの国際共同第Ⅱ相試験)
PMID 31682550: Marabell A, et al.JClinOncol2020;38:1-10 本試験はMSD社の資金提供により行われた。
●KEYNOTE-177試験 (MSI-High結腸・直腸癌を対象としたペムブロリズマブの国際共同第Ⅲ相試験)
PMID33264544:AndréT,etal.NEnglJMed.2020;383 : 2207-18. 本試験はMSD社の資金提供により行われ、 論文の著者に同社の社員、 及び著者に同社から顧問料や講演料などを受領している者が含まれる。
上記試験の結果を受けて、 本邦においてペムブロリズマブは 「がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性 (MSI-High) を有する固形癌 (標準的な治療が困難な場合に限る) 」 及び 「治癒切除不能な進行・再発の高頻度マイクロサテライト不安定性 (MSI-High) を有する結腸・直腸癌」 として承認を取得している。
MSI-Highがん種別頻度
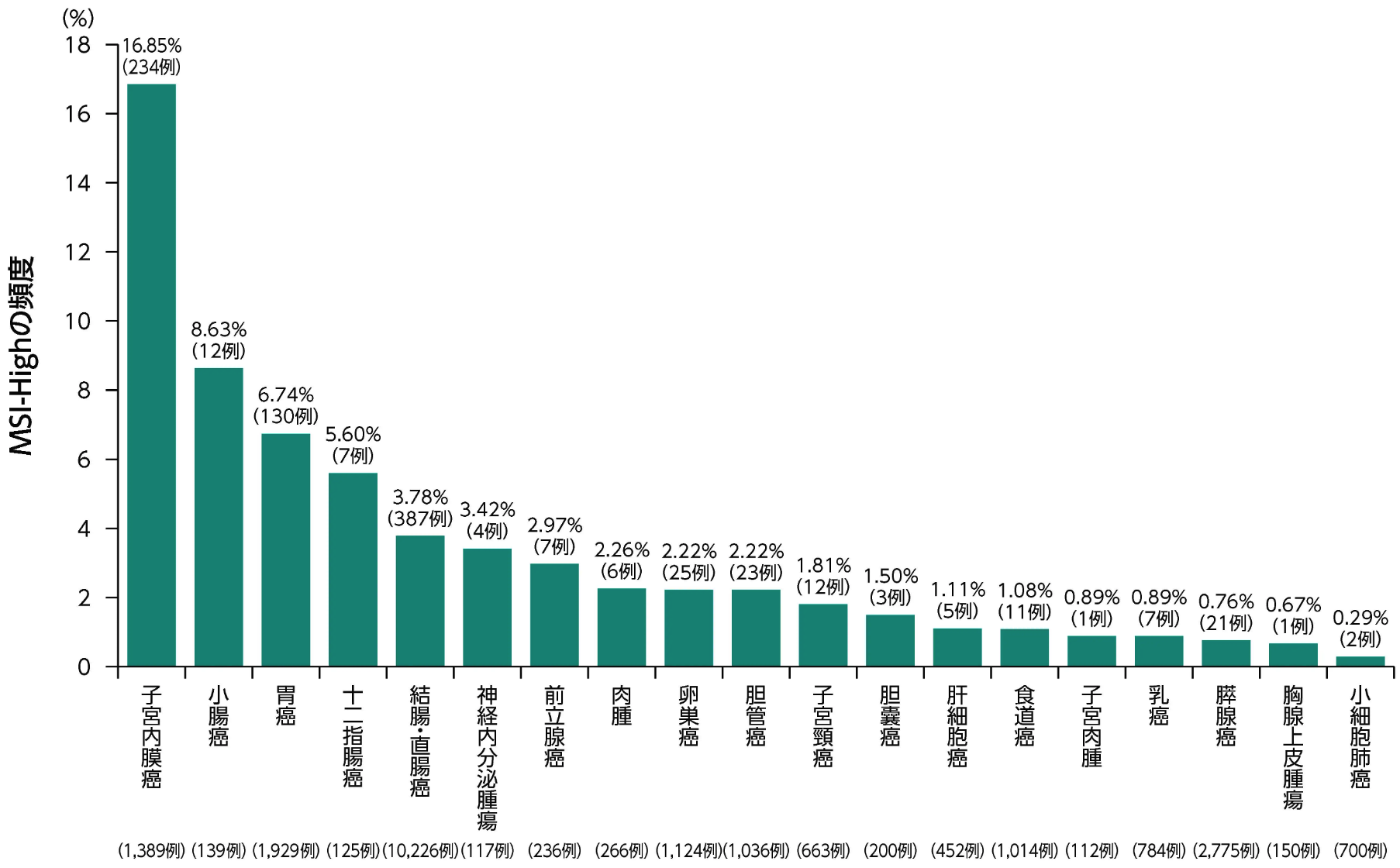
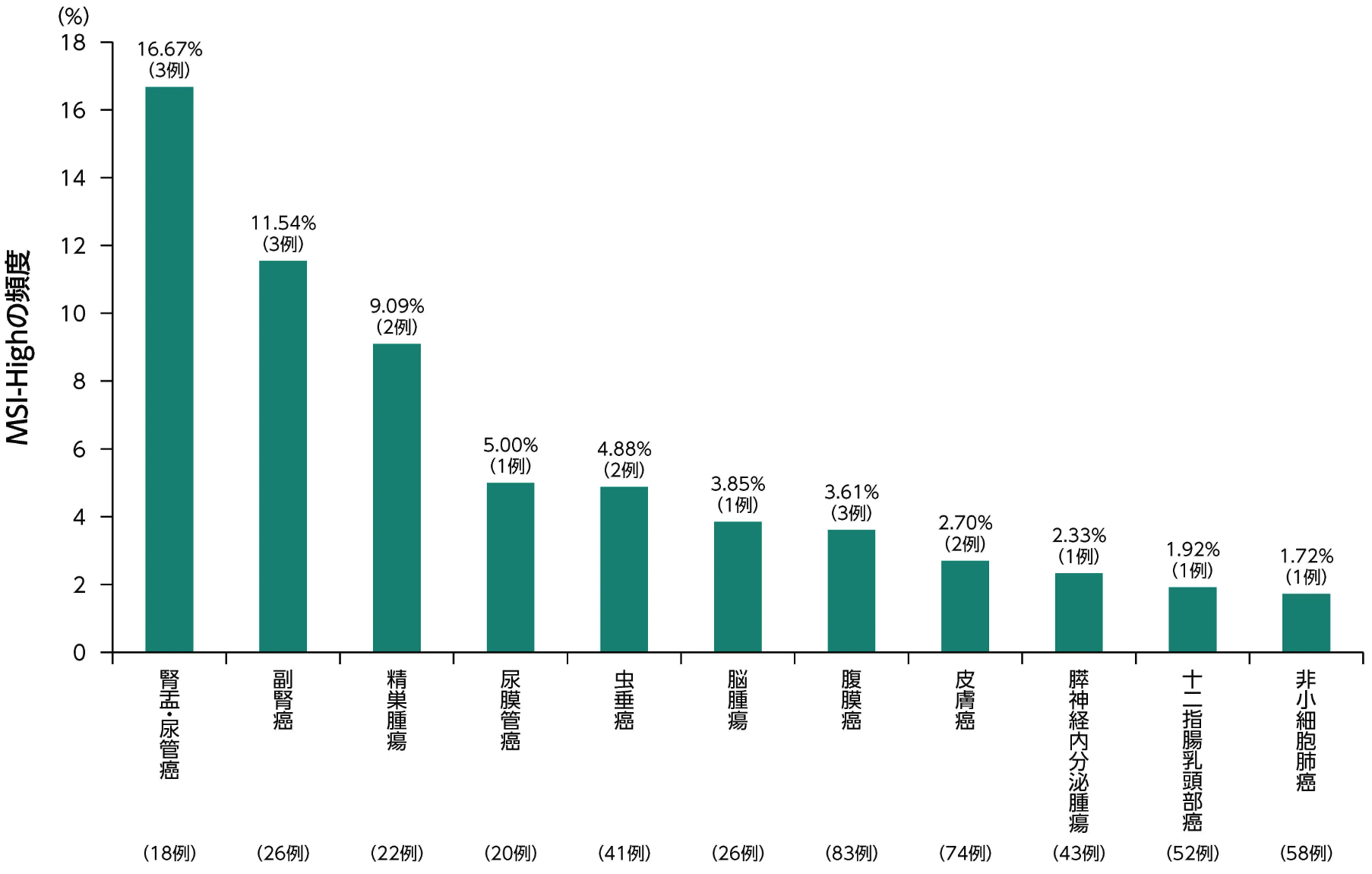
日本人の切除不能又は転移性の固形がん患者26,469例を対象とした解析により、 30のがん種においてMSI-Highが検出された¹⁾。 海外データ²⁾と同様に消化器癌、 婦人科癌で比較的頻度が高く、 検体数100以上のがんでは、 子宮内膜癌、 小腸癌、 胃癌、 十二指腸癌の順で頻度が高かった。
検体数100以上
検体数100未満

引用文献
1) Akagi K et al. Cancer Sci 2021; 112: 1105-1113. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
2) Le DT et al. Science 2017; 357: 409-413. 本試験で使用した治験薬はMSD社より提供された。 MSD社は投稿前の本試験のプロトコール及び最終原稿をレビューした。 Dung T. LeはMSD社よりコンサルタント料を受領している。 Aleksandra D. Eyring、 Bao H. Lam、 Andrew Joe、 S. Peter KangはMSD社の社員である。
dMMR判定検査法
検査の種類
MSI/MMRステータスを調べる検査には、 PCR (MSI)、 IHC (MMR)、 NGS (MSI) の3種類の手法がある。 本邦において免疫チェックポイント阻害剤のコンパニオン診断薬として位置付けられている検査の一覧とそれぞれの検査の使用目的や特徴を下記に示した。

保険点数 (MSI検査、 MMR IHC検査) ¹⁾²⁾

MSI/MMR機能検査は悪性腫瘍の治療選択を目的として行う場合であっても、 その結果はリンチ症候群診断のきっかけとなり得ます。 日本遺伝性腫瘍学会では、 検査を行うにあたっては、 一般的な悪性腫瘍に係る検査と同様に通常の医療行為としての必要な説明を行い、 検査の結果dMMR腫瘍であることが明らかとなった場合はリンチ症候群に関する情報提供を十分に行う旨の見解を示しています。
- 日本遺伝性腫瘍学会 「悪性腫瘍に対するマイクロサテライト不安定性検査およびミスマッチ修復タンパク質に対する免疫組織化学検査の利用に関する見解 ver.2」 (2023年9月) (2025/7/25閲覧)
MSI検査及びMMR IHC検査における患者説明、 遺伝カウンセリングについては 「リンチ症候群の検査・診断と遺伝カウンセリング」 をご参照ください。
MSI検査の実際
MSI検査の流れ
MSI検査は、 手術 (生検) 検体又は保存検体の①薄切、 ②病理医による切片の適切性の確認、 ③DNA抽出、 ④PCR、 ⑤電気泳動、 波形表示、 ⑥判定・レポートというフローで行う。 ①と②は各施設で行い、 ③以降は検査会社に外注するケースも多い。
MSI検査の判定¹⁾
5種類のMSIマーカーのうち、 MSI+と識別されたMSIマーカーの数が2~5個の場合は 「陽性 (MSI-High) 」、 0個 (MSS) 又は1個 (MSI-Low) の場合は 「陰性」 と判定される。
QMVR法に基づく腫瘍部位のみを用いたMSI検査の判定

再検査の基準¹⁾
明らかなMSI+は2個未満だが、 下記の 「判定に注意を要する泳動パターン例」 のマーカーを合わせると2個以上になる場合は再検査を行う。
判定に注意を要する泳動パターン例

再検査の方法¹⁾
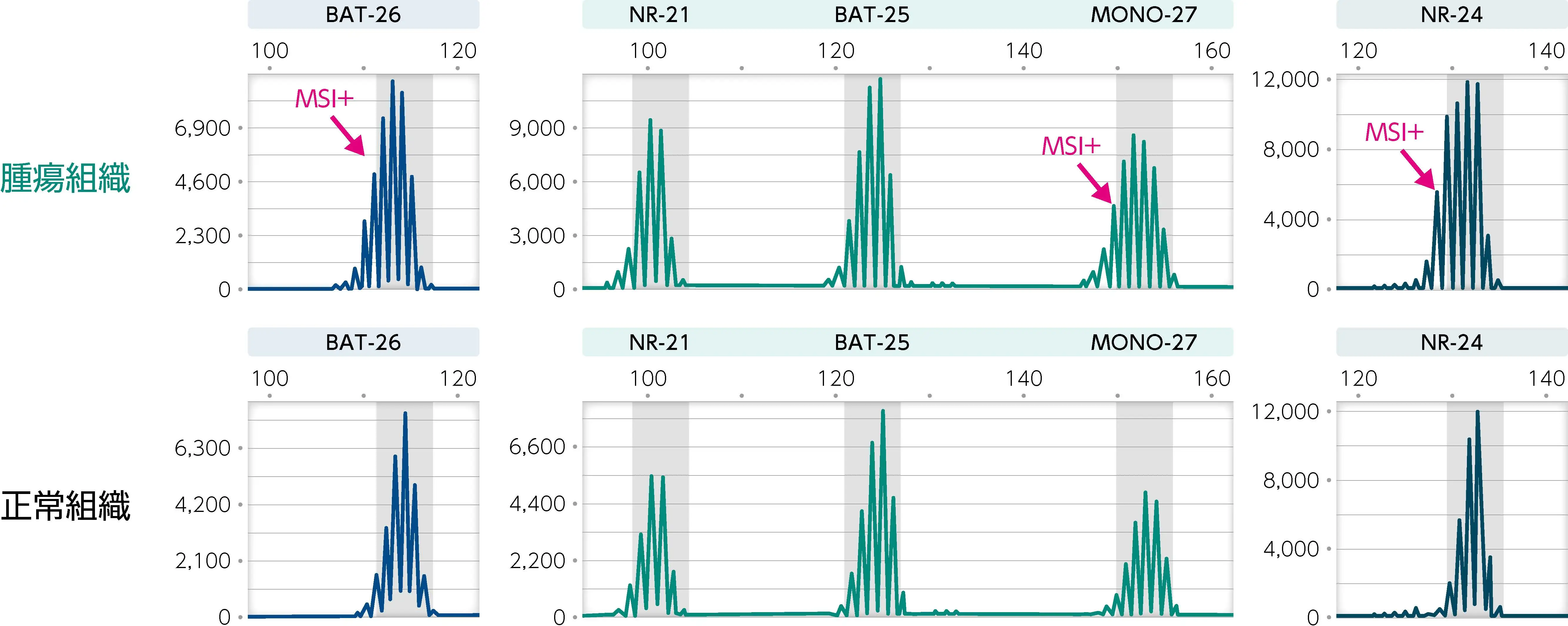
提出済みのFFPEスライドからマクロダイセクションで正常組織を採取し、 DNAを抽出して再検査を行う。 これを正常組織対照として、 腫瘍組織より得られた泳動パターンと比較し、 正常組織でも同様の波形がみられる場合はMSI-とし、 腫瘍組織のみ変化を認める場合はMSI+とする。
なお、 正常部位が腫瘍部位とともに提出されていなかった場合は、 新たに血液検体を採取して再提出する。 この血液検体からDNAを抽出し、 正常組織DNA対照として再検査を行う。
再検査における正常組織と腫瘍組織の比較 (再検査によりMSI-Highと判定された例)
FFPE検体作製における精度管理のポイントと取扱いの留意点²⁾
FFPE検体は、 室温下における長期保管やレトロスペクティブ解析に有用である一方、 検体の取り扱い方法により検体の品質差が生じやすい。 各施設におけるこれらの情報 (条件) の把握は検体を採取・提出する臨床医、 標本作製担当者及びその管理者においては不可欠である。
FFPE検体を用いた分子診断のプレアナリシス段階における主な影響因子

MSI検査のプレアナリシス段階における検体取扱いの留意点

引用文献
1) MSI検査キット (FALCO) 電子添文 2023年6月改訂 (第7版)
2) 日本病理学会編 : ゲノム研究用・診療用病理組織検体取扱い規程, 2019, 羊土社, p126-137
MMR IHC検査の実際
MMR IHC検査の流れ
MMR IHC検査は、 ホルマリン固定パラフィン包埋された組織検体の①薄切、 ②乾燥、 ③一次抗体反応、 ④スライド上のリンカー-HQ、 マルチマー-HRP反応、 ⑤DAB反応、 染色、 ⑥判定というフローで行うが、 通常③~⑤は自動染色装置で行われる。
スライドの評価可能基準及びMMR機能に対する判定基準
腫瘍組織を伴うスライドの評価可能基準及び評価不能基準

MMR機能に対する判定基準

MMR IHC検査の判定例
MMR欠損のない大腸癌 (pMMR)
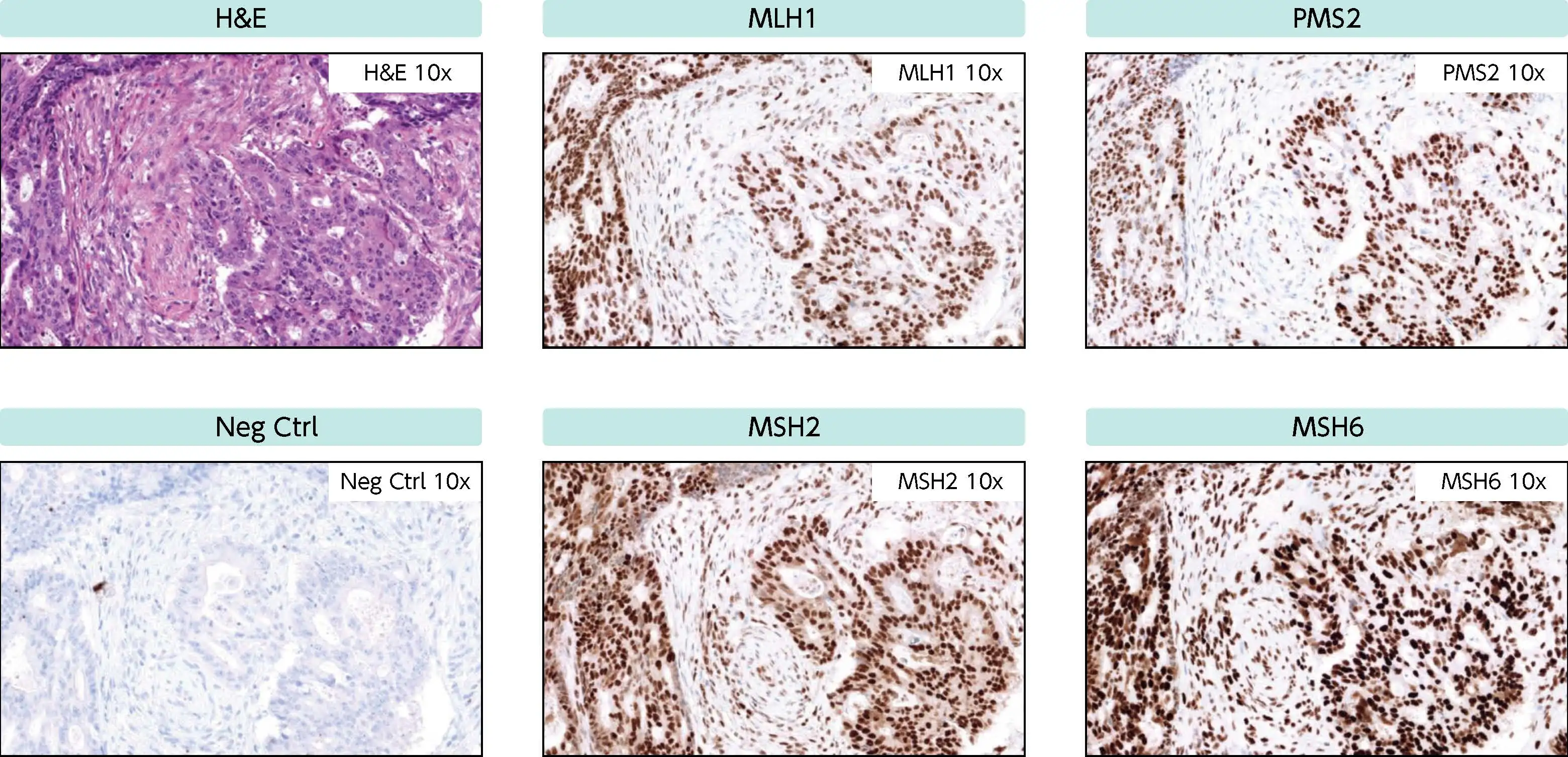
腫瘍細胞・間質の細胞 (リンパ球や線維芽細胞など) の核が均一に強陽性を示した。
MSH6欠損の大腸癌 (dMMR)
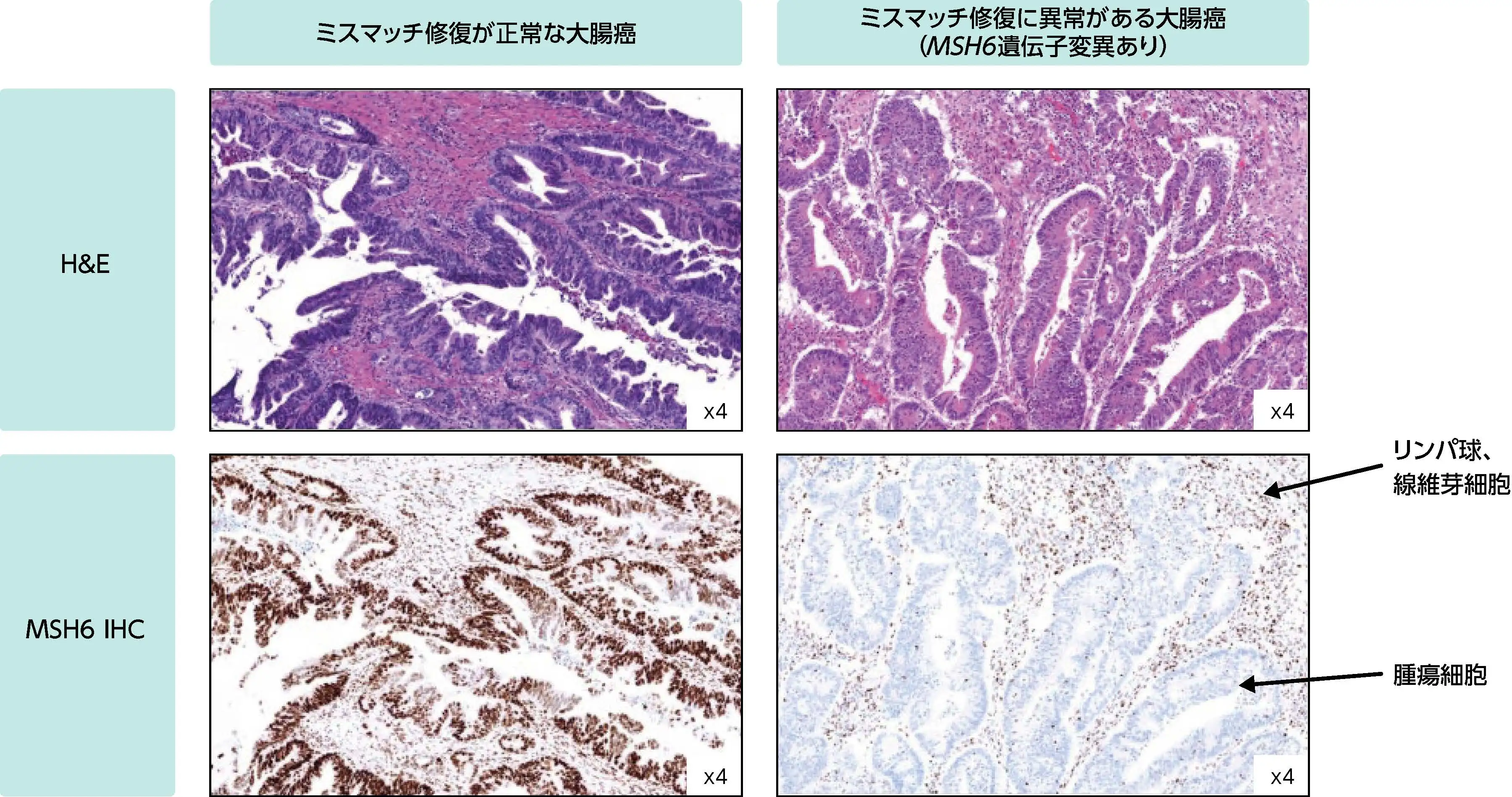
腫瘍細胞の核が陰性化した (間質の細胞は陽性)。
MMR IHC検査の染色パターン
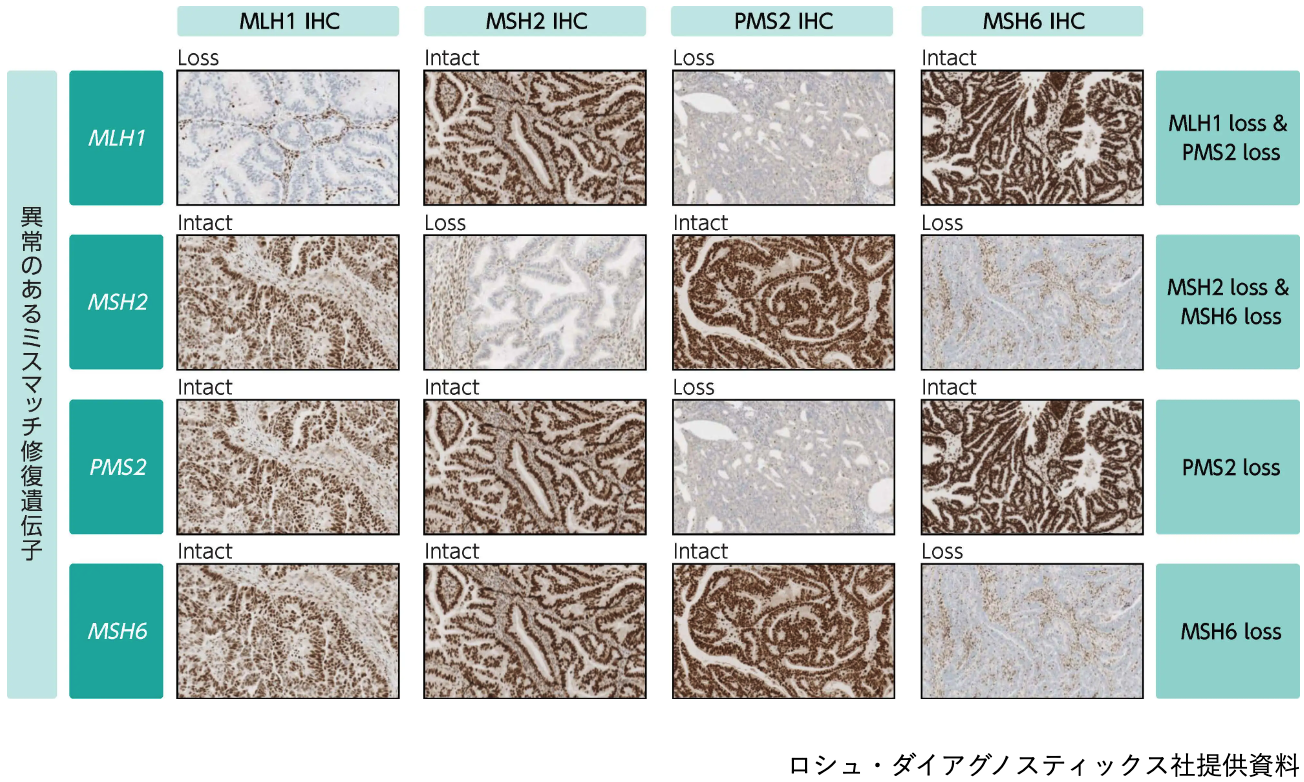
MMR IHC検査のプレアナリシス段階における検体取扱いの留意点

各種dMMR判定検査の一致率
検査の種類
MSI/MMRステータスの検査には、 ①5種類のマイクロサテライトマーカーで対立遺伝子座のサイズを調べるPCR法を用いたMSI検査、 ②がん組織中のMMRタンパク質の発現の有無を調べるIHC MMR検査、 ③がん細胞の遺伝子異常を網羅的に解析するNGSを用いたがん遺伝子パネル検査がある。 いずれの検査法も90%を超える一致率が認められている¹⁻⁶⁾。

MSI : microsatellite instability dMMR : deficient MMR IHC : 免疫組織化学染色 PCR : Polymerase Chain Reaction NGS : 次世代シーケンシング
MMR IHC検査と他の検査法の相関性¹²⁾
MMR IHC検査と他の検査法の相関性を検討した結果、 PCR法によるMSI検査、 NGS法による遺伝子検査のいずれにおいても90%を超える相関性が示された。
MSI検査とMMR IHC検査の相関性 (大腸癌及び固形がん)



遺伝子検査とMMR IHC検査との相関性¹²⁾
dMMR判定における遺伝子検査とIHC法の相関性

MLH1タンパク検出における遺伝子検査とIHC法の相関性


引用文献
1) Richman S. Int J Oncol 2015; 47: 1189-1202.
2) Dudley JC et al. Clin Cancer Res 2016; 22: 813-820.
3) Bartley AN et al. Cancer Prev Res 2012; 5: 320-327.
4) Lee V et al. Oncologist 2016; 21: 1200-1211. 本論文の著者にMSD社よりコンサルタント料を受領している者が含まれる。
5) Funkhouser Jr WK et al. J Mol Diag 2012; 14: 91-103.
6) Stelloo E et al. Ann Oncol 2017; 28: 96-102.
7) Willis J et al. Clin Cancer Res 2019; 25:7035-7045. 本論文の著者にMSD社よりコンサルタント料等を受領している者が含まれる。
8) Vanderwalde A et al. Cancer Med 2018; 7: 746–756.
9) Hempelmann J et al. J Immunother Cancer 2018; 6: 29.
10) 日本臨床腫瘍学会 / 日本癌治療学会 / 日本小児血液・がん学会編 : 成人・小児進行固形がんにおける臓器横断的ゲノム診療のガイドライン第3版, 金原出版, pp9-38, 2022.
11) Trabucco SE et al. J Mol Diagn 2019; 21: 1053-1066.
12) ベンタナ OptiView MLH1 (M1) 電子添文 2025年2月改訂 (第5版)
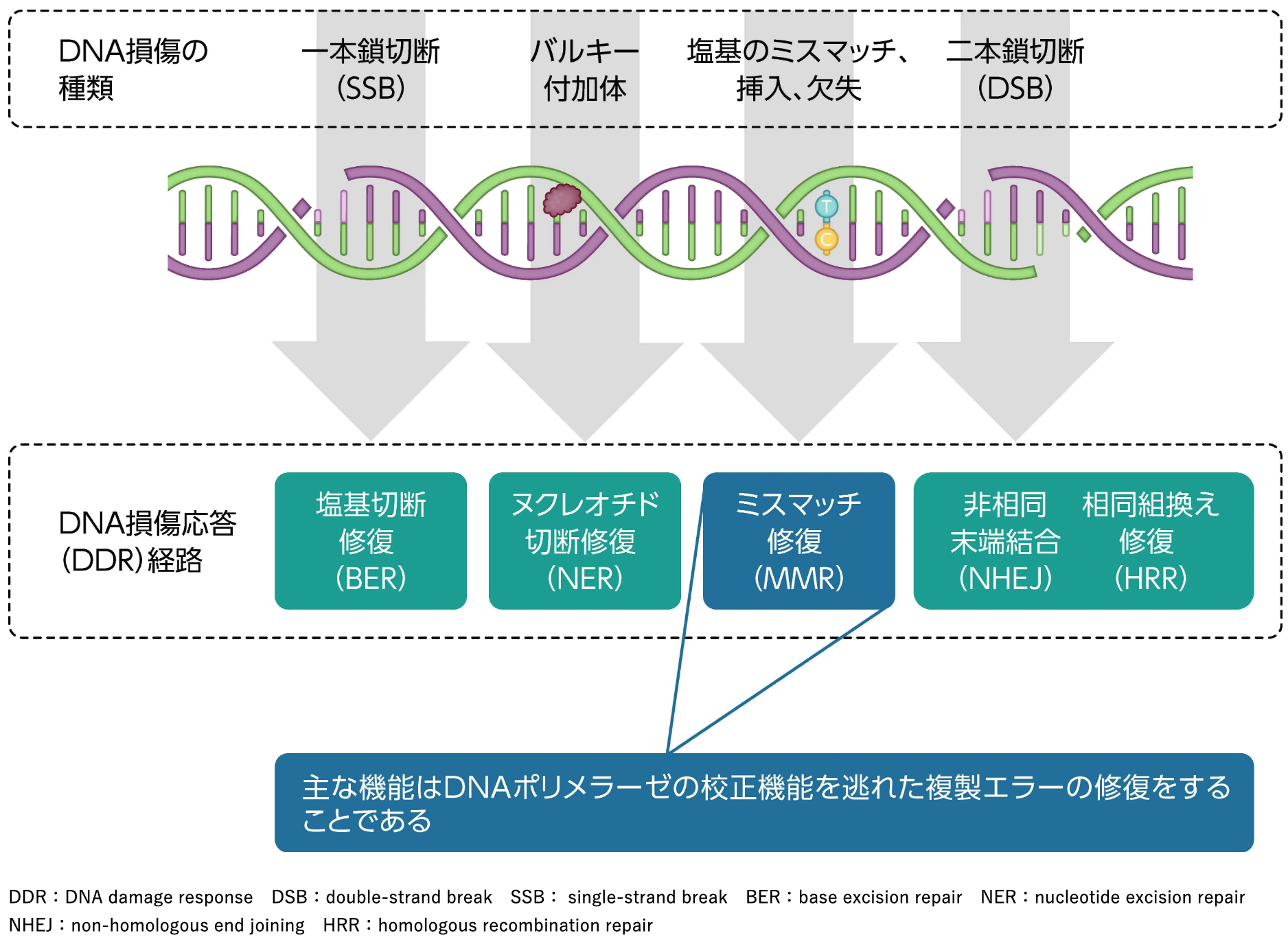
DNA損傷の種類と活性化されるDDR経路
DNAの損傷の種類により、 それぞれ活性化されるDNA損傷応答 (DDR) 経路が異なる¹⁻³⁾。 DNA複製時に生じた塩基のミスマッチや挿入・欠失は、 MMRタンパク質の複合体の機能などによって正常に修復される⁴⁾。
引用文献
1) Lord CJ et al. Nature 2012; 481: 287-294.
2) O’Conner MJ. Mol Cell 2015; 60: 547-560.
3) Ferguson LR et al. Semin Cancer Biol 2015: S5-S24.
4) Jalal S et al. Clin Cancer Res 2011; 17: 6973-6984.
固形がんにおけるMSI、 TMB及びPD-L1の関係
固形がん26種におけるTMB、 MSI及びPD-L1検査結果の重複状況 (海外データ)
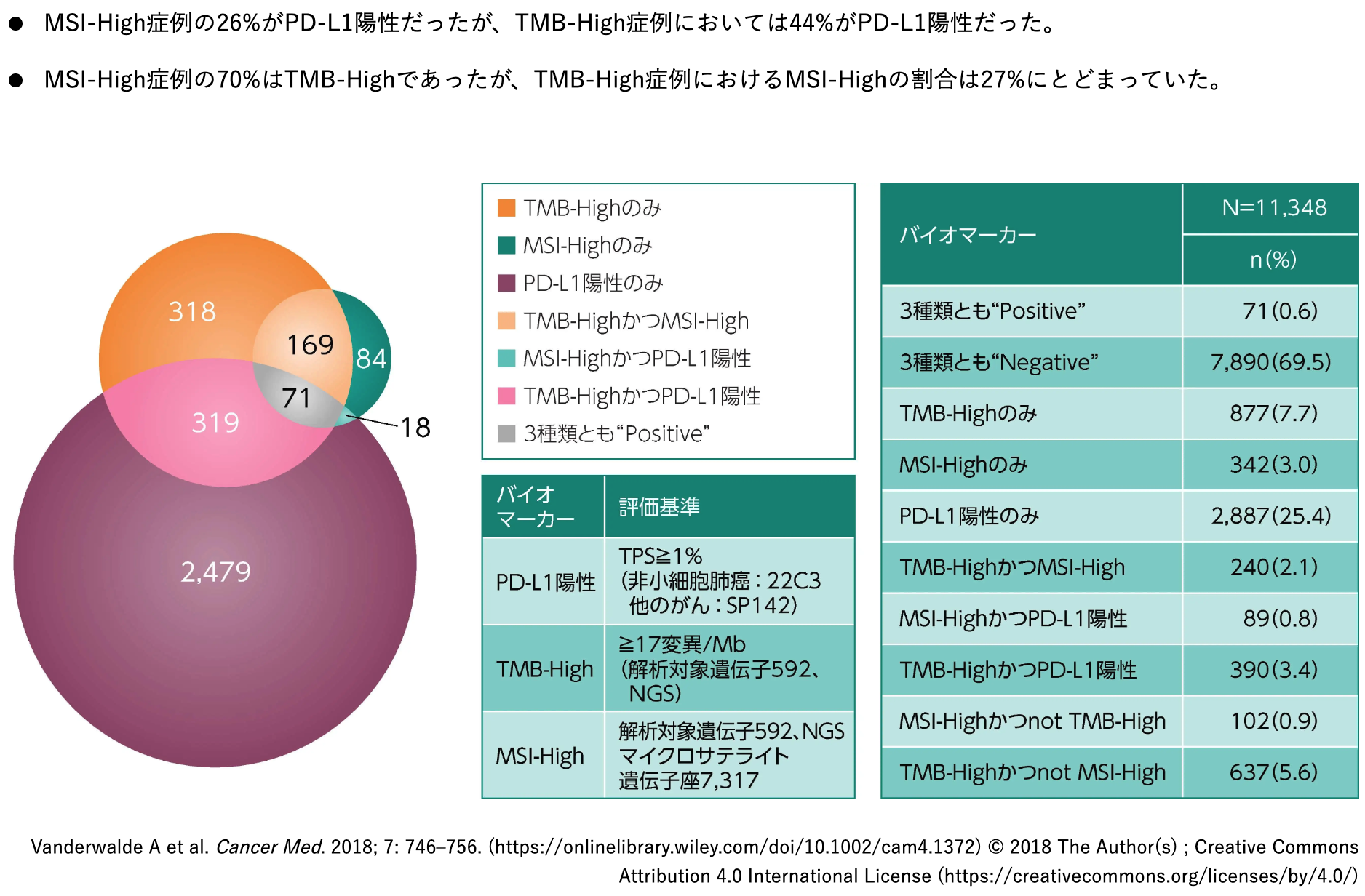
固形がん26種、 計11,348例のNGS解析結果とPD-L1 IHC検査結果を用いて、 個々の検体におけるMSI及びTMB、 PD-L1の重複状況を後ろ向きに検討した。
TMB、 MSI、 PD-L1の重複状況 (全体)
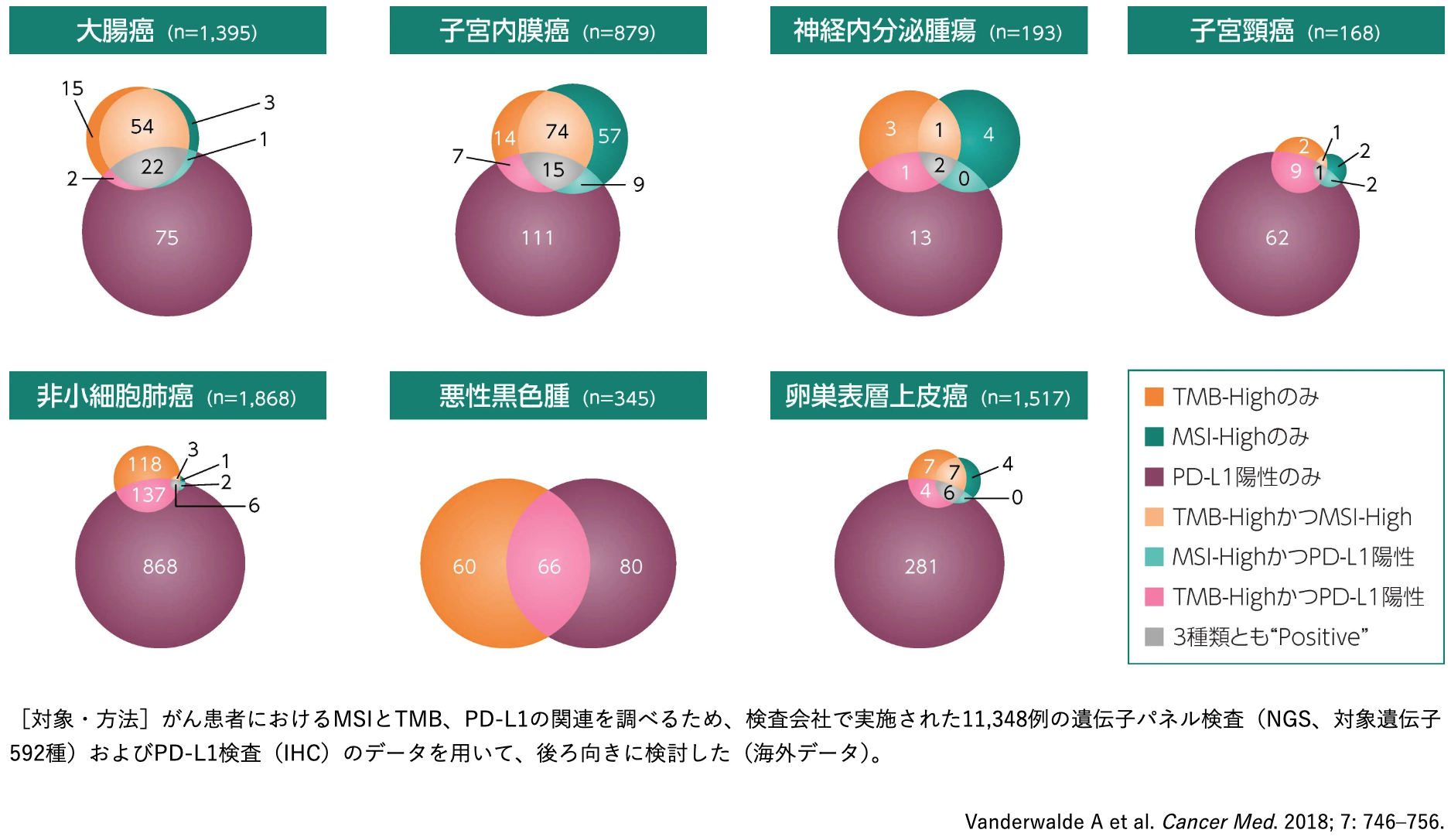
がん種別の重複状況
がん種によって3種類のマーカーの重複状況は異なり、 大腸癌、 子宮内膜癌ではMSI-HighとTMB-Highの重複例が多く認められた。 非小細胞肺癌及び悪性黒色腫では、 MSI-Highは0.6%、 0%とごく少数であったが、 TMB-Highは14.1%、 36.5%に認められた。
MSI-High/dMMRと遺伝性腫瘍
MSI検査は遺伝性疾患を特定する検査ではない
MSI検査によって検出されるMSI-Highは、 後天的な遺伝子異常と、 先天的な遺伝子異常が原因となっている場合がある。 リンチ症候群の確定診断にはさらなる遺伝学的検査などが必要となる¹⁾。

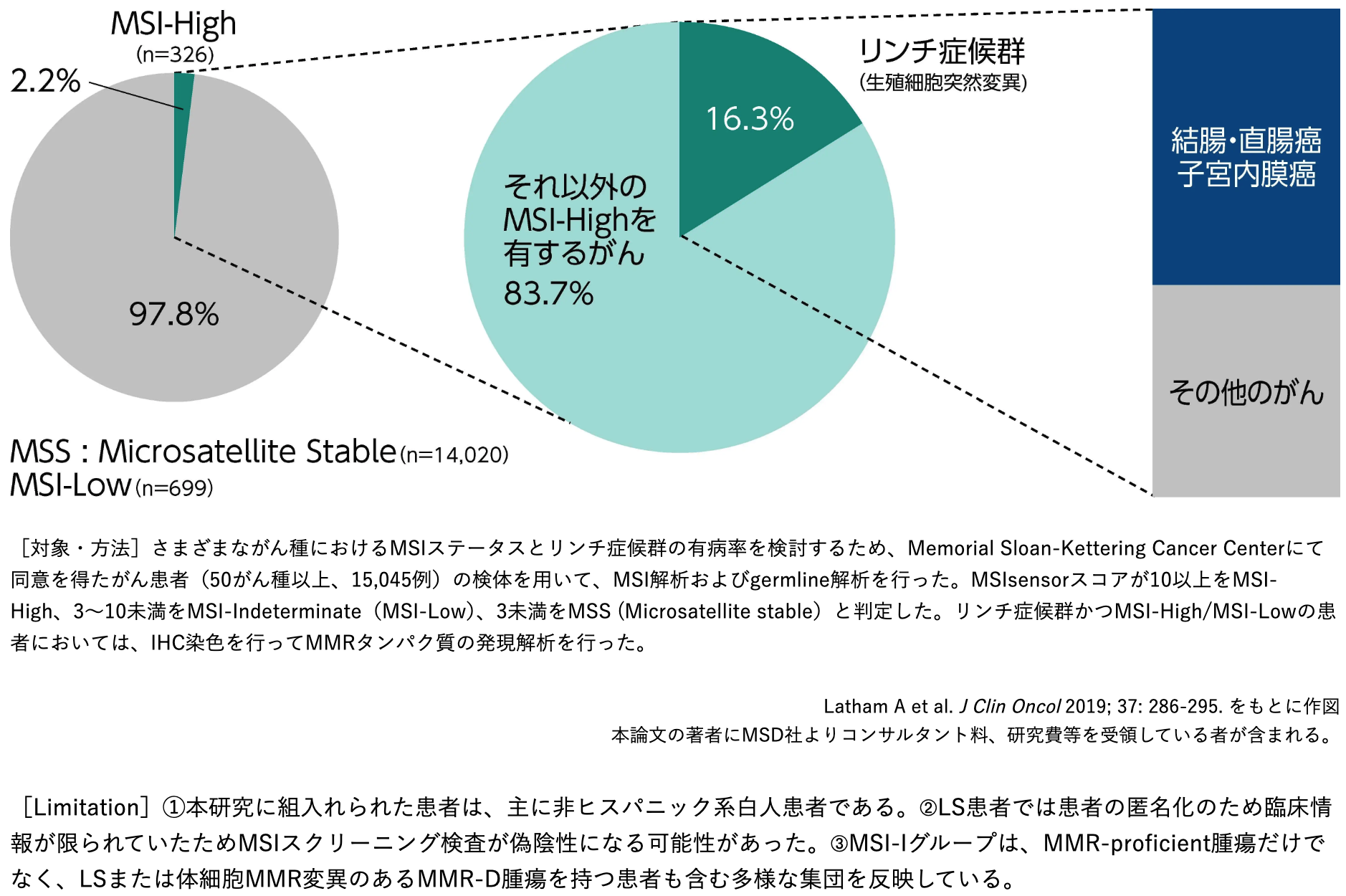
MSI-High固形がんにおけるリンチ症候群の割合 (海外データ)
固形がん15,045例の検体を用いたMSIの検討では、 MSI-Highを有する患者は全体の2.2% (326例) であった。 このうち生殖細胞の変異を有するリンチ症候群の患者は16.3%であり、 その半数以上は大腸癌及び子宮内膜癌であった²⁾。
引用文献
1) 大腸癌研究会編, 遺伝性大腸癌診療ガイドライン2024年版. 金原出版, pp87 2024.
2) Latham A et al. J Clin Oncol 2019; 37: 286-295. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
リンチ症候群の検査・診断と遺伝カウンセリング
リンチ症候群の診断フローとMSI/MMR IHC検査の位置付け
通常、 家族歴などを含む臨床病理学的情報からリンチ症候群が疑われる場合、 ①アムステルダム基準/改訂ベセスダガイドラインによる第一次スクリーニング*、 ②MSI/MMR IHC検査による第2次スクリーニング、 ③確定診断としての遺伝学的検査、 の順で診断を行う¹⁾。
*欧米では全て (または70歳未満) の大腸癌や子宮内膜癌に対し、 MSI検査またはMMR IHC検査を行うユニバーサルスクリーニングがリンチ症候群の診断に関し、 感度と費用対効果の高い方法として推奨されている。
リンチ症候群の診断手順

アムステルダム基準Ⅱ (1999) ²⁾

改訂ベセスダガイドライン (2004) ³⁾

悪性腫瘍の治療選択を目的としたMSI/MMR IHC検査を実施する際の患者説明と遺伝カウンセリングについて
日本遺伝性腫瘍学会では、 MSI/MMR IHC検査の実施にあたっては、 リンチ症候群のスクリーニングを目的として行う場合を含め、 一般的な悪性腫瘍に係る検査と同様に通常の医療行為としての必要な説明や診療録への記載を行うこととしている⁴⁾。 リンチ症候群の有病率は低く、 MSI-Highであっても多くの患者はリンチ症候群ではない⁵⁾ことから、 検査の結果dMMR腫瘍であることが明らかとなった場合はリンチ症候群に関する情報提供を十分に行うことが望まれる⁴⁾。
日本遺伝性腫瘍学会による患者説明、 遺伝カウンセリングに関する見解 (抜粋) ⁴⁾

Advisor’s comment
MSI-High/dMMRの場合のリンチ症候群である可能性は、 がん種、 家族歴、 発症年齢など複数の臨床所見を考慮する必要がある。 担当医は当該患者に必要な情報を提供し、 日本遺伝性腫瘍学会からの見解に従い 「結果が陽性であった場合にはミスマッチ修復遺伝子の遺伝子検査が受けられる機会の提供、 あるいは自施設での実施が困難な場合には、 対応可能な施設を紹介する等の配慮」 を行うことが求められる。
(国立がん研究センター東病院 桑田 健 先生)
患者説明文書例
日本遺伝性腫瘍学会では、 ウェブサイトにMSI/MMR IHC検査の実施に際する説明文書・同意書 (参考文書) を掲載している。
・マイクロサテライト不安定性検査・ミスマッチ修復タンパク質の免疫染色検査について (患者説明文書例)、 2022年1月
https://jsht-info.jp/wp/wp-content/uploads/2022/01/fb60d6b2278ce66f2366011c7⁷d7202.pdf (2025/7/25閲覧)
・免疫チェックポイント阻害薬適応判定のためのマイクロサテライト不安定性 (MSI) 検査 (説明文書・同意書) 、 2018年12月
https://jsht-info.jp/medical_personnel/project/data/msi_agreement.html (2025/7/25閲覧)

この説明文書・同意書 (参考文書) を利用される場合は、 各施設の倫理規範や診療体制等に合わせて適宜修正し、 各医療機関の責任のもとでご利用ください。
引用文献
1) 大腸癌研究会編, 遺伝性大腸癌診療ガイドライン2024年版. 金原出版, pp87 2024.
2) Vasen HFA et al. J Clin Oncol 2000; 18(21 Suppl): 81S-92S.
3) Umar A et al. J Natl Cancer Inst 2004; 96: 261-268.
4) 日本遺伝性腫瘍学会 : 悪性腫瘍に対するマイクロサテライト不安定性検査およびミスマッチ修復タンパク質に対する免疫組織化学検査の利用に関する見解 ver.2,2023年9月.https://jsht-info.jp/wp/wp-content/uploads/2023/09/28³da4a24⁰e3a04aab229839adf7c2.pdf (2025/7/25閲覧)
5) Latham A et al. J Clin Oncol 2019; 37: 286-295. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
他のバイオマーカー検査コンテンツ




編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
MSI/MMR
記載されている各薬剤及び診断薬の詳細については、 最新の電子添文をご確認ください。 また、 承認されたコンパニオン診断薬等の最新情報については、 こちらをご確認ください。

アドバイザー : 国立がん研究センター中央病院 病理診断科 科長 谷田部 恭 先生、 国立がん研究センター東病院 遺伝子診療部門 部門長 桑田 健 先生
高頻度マイクロサテライト不安定性 (MSI-High) /ミスマッチ修復機能欠損 (dMMR) の概要
MSI/MMRとは¹⁾
通常、 DNA複製時のエラーはミスマッチ修復 (MMR) タンパク質の複合体の機能などによって正常に修復されるが、 MMR機能が欠損するとエラーが修復されず、 マイクロサテライトが通常と異なる反復回数を示すことがある。 これをマイクロサテライト不安定性 (MSI) という。

MMR機能欠損によるMSI-High/dMMR固形がんの発症³⁻⁶⁾
MMR機能が正常な状態をpMMR (proficient MMR) といい、 MMR機能が欠損した状態をdMMR (deficient MMR) という。 MMR機能が欠損した状態ではDNA複製エラーが修復されず、 がん抑制遺伝子のフレームシフト変異などが引き起こされ、 エラーを持ったままの細胞が増殖して高頻度マイクロサテライト不安定性 (MSI-High) となり、 がん化の原因となる (MSI-High/dMMR固形がん)。

引用文献
1) Weinberg BA et al. Clin Advances Hem Onc 2019; 17: 109-119.
2) Salem ME et al. Mol Cancer Res 2018; 16: 805-812.
3) 川平正博他. 腫瘍内科 2017; 20: 325-330.
4) Li SKH et al. Trends Mol Med 2016; 287-289.
5) 前原喜彦他. Cancer Frontier 2001; 3: 119-127.
6) 菅井有他. 日本臨牀 2011; 69: 84:93.
効果予測バイオマーカーとしてのMSI-High/dMMR
MSI-High/dMMRと免疫応答
MSI-High/dMMR固形がんでは、 MMR機能の欠損により、 MSS/pMMR固形がんと比べてより多くの体細胞遺伝子変異を有することが報告されている¹⁾²⁾。 それにより腫瘍特異抗原 (ネオアンチゲン) の発現が高くなり、 T細胞の認識を受けやすくなることで、 抗PD-1抗体療法の反応性が高まると考えられている³⁾。


引用文献
1) Dubley JC et al. Clin Cancer Res 2016; 22: 813-820.
2) Le DT et al. Science 2017; 357: 409-413. 本試験で使用した治験薬はMSD社より提供された。 MSD社は投稿前の本試験のプロトコール及び最終原稿をレビューした。 Dung T. LeはMSD社よりコンサルタント料を受領している。 Aleksandra D. Eyring、 Bao H. Lam、 Andrew Joe、 S. Peter KangはMSD社の社員である。
3) Boyiadzis MM et al. J Immunother Cancer 2018; 6: 35. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
4) Llosa NJ et al. Cancer Discov 2015; 5: 43-51.
5) Pardoll DM et al. Nat Rev Cancer 2012; 12: 252-264.
MSI-High/dMMRとPD-1阻害剤の有効性
MSI-High/dMMRを有する腫瘍とPD-1阻害剤の有効性については、 KEYNOTE-158試験及びKEYNOTE-177試験において検討された。
●KEYNOTE-158試験 (固形がんを対象としたペムブロリズマブの国際共同第Ⅱ相試験)
PMID 31682550: Marabell A, et al.JClinOncol2020;38:1-10 本試験はMSD社の資金提供により行われた。
●KEYNOTE-177試験 (MSI-High結腸・直腸癌を対象としたペムブロリズマブの国際共同第Ⅲ相試験)
PMID33264544:AndréT,etal.NEnglJMed.2020;383 : 2207-18. 本試験はMSD社の資金提供により行われ、 論文の著者に同社の社員、 及び著者に同社から顧問料や講演料などを受領している者が含まれる。
上記試験の結果を受けて、 本邦においてペムブロリズマブは 「がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性 (MSI-High) を有する固形癌 (標準的な治療が困難な場合に限る) 」 及び 「治癒切除不能な進行・再発の高頻度マイクロサテライト不安定性 (MSI-High) を有する結腸・直腸癌」 として承認を取得している。
MSI-Highがん種別頻度
日本人の切除不能又は転移性の固形がん患者26,469例を対象とした解析により、 30のがん種においてMSI-Highが検出された¹⁾。 海外データ²⁾と同様に消化器癌、 婦人科癌で比較的頻度が高く、 検体数100以上のがんでは、 子宮内膜癌、 小腸癌、 胃癌、 十二指腸癌の順で頻度が高かった。
検体数100以上

検体数100未満


引用文献
1) Akagi K et al. Cancer Sci 2021; 112: 1105-1113. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
2) Le DT et al. Science 2017; 357: 409-413. 本試験で使用した治験薬はMSD社より提供された。 MSD社は投稿前の本試験のプロトコール及び最終原稿をレビューした。 Dung T. LeはMSD社よりコンサルタント料を受領している。 Aleksandra D. Eyring、 Bao H. Lam、 Andrew Joe、 S. Peter KangはMSD社の社員である。
dMMR判定検査法
検査の種類
MSI/MMRステータスを調べる検査には、 PCR (MSI)、 IHC (MMR)、 NGS (MSI) の3種類の手法がある。 本邦において免疫チェックポイント阻害剤のコンパニオン診断薬として位置付けられている検査の一覧とそれぞれの検査の使用目的や特徴を下記に示した。

保険点数 (MSI検査、 MMR IHC検査) ¹⁾²⁾

MSI/MMR機能検査は悪性腫瘍の治療選択を目的として行う場合であっても、 その結果はリンチ症候群診断のきっかけとなり得ます。 日本遺伝性腫瘍学会では、 検査を行うにあたっては、 一般的な悪性腫瘍に係る検査と同様に通常の医療行為としての必要な説明を行い、 検査の結果dMMR腫瘍であることが明らかとなった場合はリンチ症候群に関する情報提供を十分に行う旨の見解を示しています。
- 日本遺伝性腫瘍学会 「悪性腫瘍に対するマイクロサテライト不安定性検査およびミスマッチ修復タンパク質に対する免疫組織化学検査の利用に関する見解 ver.2」 (2023年9月) (2025/7/25閲覧)
MSI検査及びMMR IHC検査における患者説明、 遺伝カウンセリングについては 「リンチ症候群の検査・診断と遺伝カウンセリング」 をご参照ください。
MSI検査の実際
MSI検査の流れ
MSI検査は、 手術 (生検) 検体又は保存検体の①薄切、 ②病理医による切片の適切性の確認、 ③DNA抽出、 ④PCR、 ⑤電気泳動、 波形表示、 ⑥判定・レポートというフローで行う。 ①と②は各施設で行い、 ③以降は検査会社に外注するケースも多い。
MSI検査の判定¹⁾
5種類のMSIマーカーのうち、 MSI+と識別されたMSIマーカーの数が2~5個の場合は 「陽性 (MSI-High) 」、 0個 (MSS) 又は1個 (MSI-Low) の場合は 「陰性」 と判定される。
QMVR法に基づく腫瘍部位のみを用いたMSI検査の判定

再検査の基準¹⁾
明らかなMSI+は2個未満だが、 下記の 「判定に注意を要する泳動パターン例」 のマーカーを合わせると2個以上になる場合は再検査を行う。
判定に注意を要する泳動パターン例

再検査の方法¹⁾
提出済みのFFPEスライドからマクロダイセクションで正常組織を採取し、 DNAを抽出して再検査を行う。 これを正常組織対照として、 腫瘍組織より得られた泳動パターンと比較し、 正常組織でも同様の波形がみられる場合はMSI-とし、 腫瘍組織のみ変化を認める場合はMSI+とする。
なお、 正常部位が腫瘍部位とともに提出されていなかった場合は、 新たに血液検体を採取して再提出する。 この血液検体からDNAを抽出し、 正常組織DNA対照として再検査を行う。
再検査における正常組織と腫瘍組織の比較 (再検査によりMSI-Highと判定された例)

FFPE検体作製における精度管理のポイントと取扱いの留意点²⁾
FFPE検体は、 室温下における長期保管やレトロスペクティブ解析に有用である一方、 検体の取り扱い方法により検体の品質差が生じやすい。 各施設におけるこれらの情報 (条件) の把握は検体を採取・提出する臨床医、 標本作製担当者及びその管理者においては不可欠である。
FFPE検体を用いた分子診断のプレアナリシス段階における主な影響因子

MSI検査のプレアナリシス段階における検体取扱いの留意点

引用文献
1) MSI検査キット (FALCO) 電子添文 2023年6月改訂 (第7版)
2) 日本病理学会編 : ゲノム研究用・診療用病理組織検体取扱い規程, 2019, 羊土社, p126-137
MMR IHC検査の実際
MMR IHC検査の流れ
MMR IHC検査は、 ホルマリン固定パラフィン包埋された組織検体の①薄切、 ②乾燥、 ③一次抗体反応、 ④スライド上のリンカー-HQ、 マルチマー-HRP反応、 ⑤DAB反応、 染色、 ⑥判定というフローで行うが、 通常③~⑤は自動染色装置で行われる。
スライドの評価可能基準及びMMR機能に対する判定基準
腫瘍組織を伴うスライドの評価可能基準及び評価不能基準

MMR機能に対する判定基準

MMR IHC検査の判定例
MMR欠損のない大腸癌 (pMMR)

腫瘍細胞・間質の細胞 (リンパ球や線維芽細胞など) の核が均一に強陽性を示した。
MSH6欠損の大腸癌 (dMMR)

腫瘍細胞の核が陰性化した (間質の細胞は陽性)。
MMR IHC検査の染色パターン

MMR IHC検査のプレアナリシス段階における検体取扱いの留意点

各種dMMR判定検査の一致率
検査の種類
MSI/MMRステータスの検査には、 ①5種類のマイクロサテライトマーカーで対立遺伝子座のサイズを調べるPCR法を用いたMSI検査、 ②がん組織中のMMRタンパク質の発現の有無を調べるIHC MMR検査、 ③がん細胞の遺伝子異常を網羅的に解析するNGSを用いたがん遺伝子パネル検査がある。 いずれの検査法も90%を超える一致率が認められている¹⁻⁶⁾。

MSI : microsatellite instability dMMR : deficient MMR IHC : 免疫組織化学染色 PCR : Polymerase Chain Reaction NGS : 次世代シーケンシング
MMR IHC検査と他の検査法の相関性¹²⁾
MMR IHC検査と他の検査法の相関性を検討した結果、 PCR法によるMSI検査、 NGS法による遺伝子検査のいずれにおいても90%を超える相関性が示された。
MSI検査とMMR IHC検査の相関性 (大腸癌及び固形がん)



遺伝子検査とMMR IHC検査との相関性¹²⁾
dMMR判定における遺伝子検査とIHC法の相関性

MLH1タンパク検出における遺伝子検査とIHC法の相関性


引用文献
1) Richman S. Int J Oncol 2015; 47: 1189-1202.
2) Dudley JC et al. Clin Cancer Res 2016; 22: 813-820.
3) Bartley AN et al. Cancer Prev Res 2012; 5: 320-327.
4) Lee V et al. Oncologist 2016; 21: 1200-1211. 本論文の著者にMSD社よりコンサルタント料を受領している者が含まれる。
5) Funkhouser Jr WK et al. J Mol Diag 2012; 14: 91-103.
6) Stelloo E et al. Ann Oncol 2017; 28: 96-102.
7) Willis J et al. Clin Cancer Res 2019; 25:7035-7045. 本論文の著者にMSD社よりコンサルタント料等を受領している者が含まれる。
8) Vanderwalde A et al. Cancer Med 2018; 7: 746–756.
9) Hempelmann J et al. J Immunother Cancer 2018; 6: 29.
10) 日本臨床腫瘍学会 / 日本癌治療学会 / 日本小児血液・がん学会編 : 成人・小児進行固形がんにおける臓器横断的ゲノム診療のガイドライン第3版, 金原出版, pp9-38, 2022.
11) Trabucco SE et al. J Mol Diagn 2019; 21: 1053-1066.
12) ベンタナ OptiView MLH1 (M1) 電子添文 2025年2月改訂 (第5版)
DNA損傷の種類と活性化されるDDR経路
DNAの損傷の種類により、 それぞれ活性化されるDNA損傷応答 (DDR) 経路が異なる¹⁻³⁾。 DNA複製時に生じた塩基のミスマッチや挿入・欠失は、 MMRタンパク質の複合体の機能などによって正常に修復される⁴⁾。

引用文献
1) Lord CJ et al. Nature 2012; 481: 287-294.
2) O’Conner MJ. Mol Cell 2015; 60: 547-560.
3) Ferguson LR et al. Semin Cancer Biol 2015: S5-S24.
4) Jalal S et al. Clin Cancer Res 2011; 17: 6973-6984.
固形がんにおけるMSI、 TMB及びPD-L1の関係
固形がん26種におけるTMB、 MSI及びPD-L1検査結果の重複状況 (海外データ)
固形がん26種、 計11,348例のNGS解析結果とPD-L1 IHC検査結果を用いて、 個々の検体におけるMSI及びTMB、 PD-L1の重複状況を後ろ向きに検討した。
TMB、 MSI、 PD-L1の重複状況 (全体)

がん種別の重複状況
がん種によって3種類のマーカーの重複状況は異なり、 大腸癌、 子宮内膜癌ではMSI-HighとTMB-Highの重複例が多く認められた。 非小細胞肺癌及び悪性黒色腫では、 MSI-Highは0.6%、 0%とごく少数であったが、 TMB-Highは14.1%、 36.5%に認められた。

MSI-High/dMMRと遺伝性腫瘍
MSI検査は遺伝性疾患を特定する検査ではない
MSI検査によって検出されるMSI-Highは、 後天的な遺伝子異常と、 先天的な遺伝子異常が原因となっている場合がある。 リンチ症候群の確定診断にはさらなる遺伝学的検査などが必要となる¹⁾。

MSI-High固形がんにおけるリンチ症候群の割合 (海外データ)
固形がん15,045例の検体を用いたMSIの検討では、 MSI-Highを有する患者は全体の2.2% (326例) であった。 このうち生殖細胞の変異を有するリンチ症候群の患者は16.3%であり、 その半数以上は大腸癌及び子宮内膜癌であった²⁾。

引用文献
1) 大腸癌研究会編, 遺伝性大腸癌診療ガイドライン2024年版. 金原出版, pp87 2024.
2) Latham A et al. J Clin Oncol 2019; 37: 286-295. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
リンチ症候群の検査・診断と遺伝カウンセリング
リンチ症候群の診断フローとMSI/MMR IHC検査の位置付け
通常、 家族歴などを含む臨床病理学的情報からリンチ症候群が疑われる場合、 ①アムステルダム基準/改訂ベセスダガイドラインによる第一次スクリーニング*、 ②MSI/MMR IHC検査による第2次スクリーニング、 ③確定診断としての遺伝学的検査、 の順で診断を行う¹⁾。
*欧米では全て (または70歳未満) の大腸癌や子宮内膜癌に対し、 MSI検査またはMMR IHC検査を行うユニバーサルスクリーニングがリンチ症候群の診断に関し、 感度と費用対効果の高い方法として推奨されている。
リンチ症候群の診断手順

アムステルダム基準Ⅱ (1999) ²⁾

改訂ベセスダガイドライン (2004) ³⁾

悪性腫瘍の治療選択を目的としたMSI/MMR IHC検査を実施する際の患者説明と遺伝カウンセリングについて
日本遺伝性腫瘍学会では、 MSI/MMR IHC検査の実施にあたっては、 リンチ症候群のスクリーニングを目的として行う場合を含め、 一般的な悪性腫瘍に係る検査と同様に通常の医療行為としての必要な説明や診療録への記載を行うこととしている⁴⁾。 リンチ症候群の有病率は低く、 MSI-Highであっても多くの患者はリンチ症候群ではない⁵⁾ことから、 検査の結果dMMR腫瘍であることが明らかとなった場合はリンチ症候群に関する情報提供を十分に行うことが望まれる⁴⁾。
日本遺伝性腫瘍学会による患者説明、 遺伝カウンセリングに関する見解 (抜粋) ⁴⁾

Advisor’s comment
MSI-High/dMMRの場合のリンチ症候群である可能性は、 がん種、 家族歴、 発症年齢など複数の臨床所見を考慮する必要がある。 担当医は当該患者に必要な情報を提供し、 日本遺伝性腫瘍学会からの見解に従い 「結果が陽性であった場合にはミスマッチ修復遺伝子の遺伝子検査が受けられる機会の提供、 あるいは自施設での実施が困難な場合には、 対応可能な施設を紹介する等の配慮」 を行うことが求められる。
(国立がん研究センター東病院 桑田 健 先生)
患者説明文書例
日本遺伝性腫瘍学会では、 ウェブサイトにMSI/MMR IHC検査の実施に際する説明文書・同意書 (参考文書) を掲載している。
・マイクロサテライト不安定性検査・ミスマッチ修復タンパク質の免疫染色検査について (患者説明文書例)、 2022年1月
https://jsht-info.jp/wp/wp-content/uploads/2022/01/fb60d6b2278ce66f2366011c7⁷d7202.pdf (2025/7/25閲覧)
・免疫チェックポイント阻害薬適応判定のためのマイクロサテライト不安定性 (MSI) 検査 (説明文書・同意書) 、 2018年12月
https://jsht-info.jp/medical_personnel/project/data/msi_agreement.html (2025/7/25閲覧)

この説明文書・同意書 (参考文書) を利用される場合は、 各施設の倫理規範や診療体制等に合わせて適宜修正し、 各医療機関の責任のもとでご利用ください。
引用文献
1) 大腸癌研究会編, 遺伝性大腸癌診療ガイドライン2024年版. 金原出版, pp87 2024.
2) Vasen HFA et al. J Clin Oncol 2000; 18(21 Suppl): 81S-92S.
3) Umar A et al. J Natl Cancer Inst 2004; 96: 261-268.
4) 日本遺伝性腫瘍学会 : 悪性腫瘍に対するマイクロサテライト不安定性検査およびミスマッチ修復タンパク質に対する免疫組織化学検査の利用に関する見解 ver.2,2023年9月.https://jsht-info.jp/wp/wp-content/uploads/2023/09/28³da4a24⁰e3a04aab229839adf7c2.pdf (2025/7/25閲覧)
5) Latham A et al. J Clin Oncol 2019; 37: 286-295. 本論文の著者にMSD社よりコンサルタント料、 研究費等を受領している者が含まれる。
他のバイオマーカー検査コンテンツ




編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
あなたは医師もしくは医療関係者ですか?
HOKUTOへようこそ。当サイトでは、医師の方を対象に株式会社HOKUTOの臨床支援コンテンツを提供しています。




